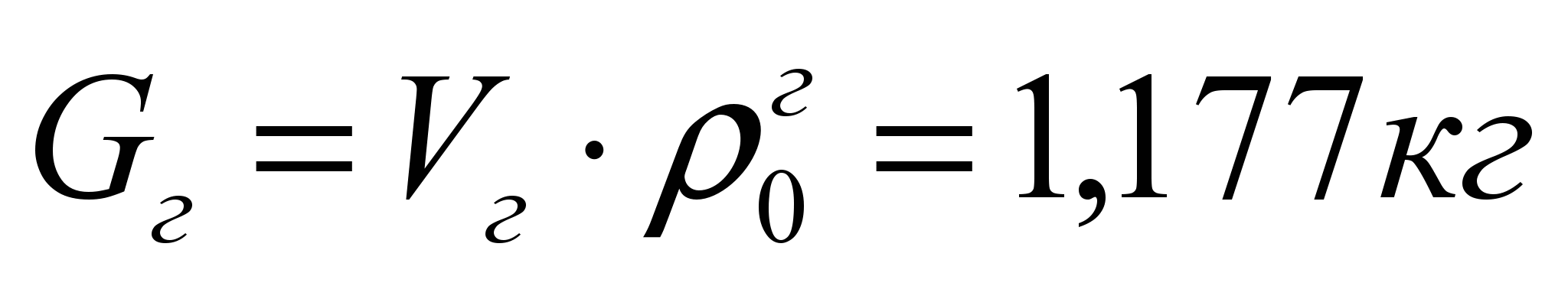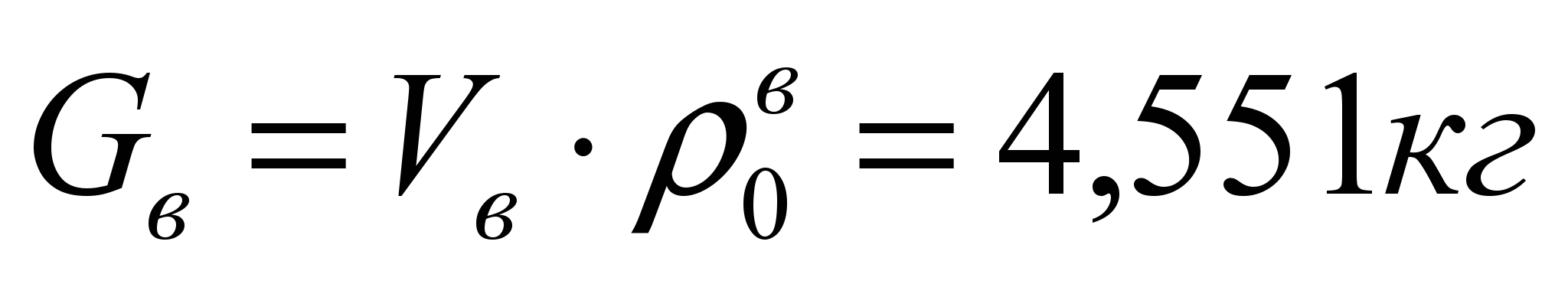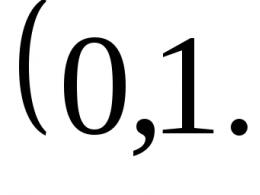Расчет горения угольной пыли. Введение
4.7. Расчет горения органического топлива
Расчет сводится к определению количества воздуха, необходимого для полного сгорания топлива, продуктов горения, а также температуры и энтальпии дымовых газов. Расчет твердого и жидкого топлива ведут по соотношениям масс веществ, участвующих в реакциях, а для газообразного топлива – по объемным соотношениям.
Для полного сжигания 1 кг углерода С требуется 1,866 м 3 кислорода О 2 , в результате чего образуется 1,866 м 3 двуокиси углерода СО 2 и выделяется 34 МДж (34 000 кДж) теплоты:
С + О 2 = СО 2 + Q .
Для полного сгорания 1 кг серы S требуется 0,7 м 3 кислорода О 2 , в результате образуется 0,7 м 3 сернистого газа SО 2 и выделяется 10,5 МДж теплоты:
S + О 2 = SО 2 + Q .
Для полного сгорания 1 кг водорода Н 2 требуется 5,6 м 3 кислорода О 2 , образуется 11,2 м 3 водяного пара Н 2 О и выделяется 121,5 МДж теплоты:
2Н 2 + О 2 = 2Н 2 О + Q .
Для полного сгорания 1 м 3 метана СН 4 требуется 9,52 м 3 воздуха V о, образуется 10,52 м 3 дымовых газов, содержащих СО 2 и водяные пары Н 2 О, и выделяется 36,5 МДж теплоты:
СН 4 + 2О 2 = СО 2 + 2Н 2 О + Q .
При полном сгорании топлива дымовые газы содержат углекислый газ СО 2 , сернистый газ SО 2 , азот топлива и воздуха N 2 , неиспользованный при горении кислород О 2 воздуха, водяной пар Н 2 О, полученный за счет окисления водорода топлива, испарения влаги, содержащейся в топливе и внесенной с влажным воздухом и при распылении жидкого топлива (в паромеханических форсунках).
Для полного горения топлива необходимы: достаточное количество воздуха; хорошее перемешивание воздуха с топливом; высокая температура в топке (не менее 700 °С на выходе); достаточное время пребывания топлива и окислителя в топке; постоянный отвод продуктов сгорания из топки.
При неполном сгорании топлива образуются вредные для человека и окружающей среды оксиды азота (NО, NО 2), серы (SО 2), углерода СО (угарный газ), а также сажа, которая осаждается на экранных и конвективных трубах, снижает теплопередачу от топочных газов к теплоносителю, что приводит к уменьшению КПД и перерасходу топлива. Кроме того, сажа может самовозгораться, что приводит к авариям.
Полнота сгорания топлива определяется двумя способами:
1) с помощью газоанализаторов – по показаниям состава уходящих топочных газов оценивается полнота сгорания и избыток воздуха;
2) визуально – по цвету пламени и дыма. При полном сгорании цвет пламени в разогретой топке голубовато-фиолетовый или прозрачно-соломенный, а цвет дыма – бесцветный, прозрачный, невидимый для глаза – летом и светло-серый или белый – зимой. При неполном сгорании цвет пламени оранжево-красный, с темными язычками, непрозрачный, а цвет дыма – серый ближе к темному, непрозрачный.
Энтальпия воздуха и продуктов сгорания зависит от объема, теплоемкости и температуры компонентов горения и вычисляется по формулам, после чего строится график зависимости энтальпии от температуры топочных газов для каждого элемента котла (топки, газоходов, пароперегревателя, экономайзера и т.п.).
Различают теоретическую (калориметрическую) и действительную температуру горения топлива.
Максимальную температуру, развиваемую при сжигании топлива, называют жаропроизводительностью топлива. Теоретическая – это та температура, которую приобрели бы дымовые газы, если бы вся теплота от полного сгорания топлива воспринималась бы только дымовыми газами. Калориметрическую температуру горения определяют из уравнения теплового баланса. В реальных условиях горения топлива действительная температура топочных газов всегда ниже теоретической за счет теплообмена между топочными газами и радиационными поверхностями нагрева, а также различных потерь теплоты в топке (механический, химический недожог и др.).
4.8. Коэффициент избытка воздуха
Для обеспечения полного сгорания топлива в топочное устройство подводят воздуха больше, чем теоретически необходимо. Отношение действительно поступившего количества воздуха V д к теоретически необходимому V о, называется коэффициентом избытка воздуха α т.
Топки паровых и водогрейных котлов, как правило, работают с разрежением 2…3 мм вод. ст., в связи с чем происходит подсос воздуха и в топку и во все элементы котельной установки по ходу газового тракта, вплоть до дымососа. Присосы воздуха для каждого элемента котла определяются по и ориентировочно могут быть приняты:
0,05 – для первого конвективного пучка (газохода), фестона (с камерой догорания), пароперегревателя, воздухоподогревателя;
0,1 – для второго конвективного пучка (газохода), конвективной шахты, чугунного и стального экономайзера с обшивкой;
0,15…0,2 – для чугунного экономайзера без обшивки.
Поэтому коэффициент избытка воздуха в уходящих топочных газах – αух больше чем в топке, на суммарное значение присосов воздуха ΣΔα и составляет:
α ух = α т + ΣΔα.
Разрежение в топке замеряется тягонапоромером ТНЖ. При разрежении менее 1 мм вод. ст. топочные газы могут выбиваться в помещение котельной, что недопустимо по технике безопасности. При разрежении более 8 мм вод. ст. будет происходить значительный подсос холодного наружного воздуха, что приведет к снижению температуры топочных газов, увеличению потерь теплоты, снижению КПД и др.
5. Тепловой баланс теплогенератора
5.1. Уравнение теплового баланса
Расход сжигаемого топлива должен обеспечивать получение необходимого количество полезной теплоты, а также восполнение тепловых потерь, сопровождающих работу котельной установки. Полезно используемая теплота в котельной установке Q 1 идет на подогрев воды, ее испарение, получение и перегрев пара. Соотношение, связывающее приход и расход теплоты, носит название теплового баланса .
Тепловой баланс составляется на 1 кг твердого или жидкого топлива, на 1 м 3 газообразного топлива или в % от введенной теплоты. Суммарное количество введенной в топку теплоты называется располагаемой теплотой Q р р и соответственно включает в себя:
Q р н – низшую рабочую теплоту сгорания топлива;
Q ф.т – физическую теплоту, вводимую в теплогенератор с топливом, если топливо предварительно нагревается (мазут);
Q ф.в – физическую теплоту, вводимую в теплогенератор с воздухом, если нагрев воздуха происходит вне котельного агрегата (воздухоподогреватель);
Q пар – физическую теплоту, вводимую в теплогенератор с паром, при паровом распылении топлива (паромеханические форсунки).
Следовательно,
Q р р = Q р н + Q ф.т + Q ф.в + Q пар.
Расходная часть теплового баланса Q расх включает в себя полезно использованную теплоту Q 1 , а также потери теплоты с уходящими топочными газами Q 2 , химической Q 3 и механической Q 4 неполнотой сгорания топлива, от наружного охлаждения Q 5 , с физической теплотой шлаков Q 6 , на аккумуляцию ограждающих конструкций Q ак (при нестационарных условиях работы установки). Следовательно,
Q расх = Q 1 + Q 2 + Q 3 + Q 4 + Q 5 + Q 6 + Q ак.
Уравнение теплового баланса имеет вид
Q р р = Q расх.
Разделив, каждый член уравнения теплового баланса на Q р р и умножив на 100 %, получим другую запись уравнения теплового баланса:
100 = q 1 + q 2 + q 3 + q 4 + q 5 + q 6 .
5.2. Коэффициент полезного действия и расход топлива
теплогенератора
Коэффициентом полезного действия брутто η бр, %, называется отношение полезно используемой теплоты Q 1 к располагаемой Q р р:
η бр = (Q 1 / Q р р) ⋅ 100, %.
Доля полезно используемой теплоты
q 1 = (Q 1 / Q р р) 100, %.
Тогда имеем, что q 1 = η бр.
Следовательно, коэффициент полезного действия брутто
η бр = 100 − (q 2 + q 3 + q 4 + q 5 + q 6), %.
При выработке тепловой энергии следует учитывать расход тепловой энергии на собственные нужды q с.н (привод насосов, тягодутьевых устройств, на обдувку, деаэрацию, мазутное хозяйство и т.д.). В связи с этим введено понятие КПД нетто
η нетто = η бр − q с.н, %.
Натуральный расход топлива В н, кг/с, м 3 /с, при нормальных условиях сжигания (при t = 0 °С и Р = 760 мм рт. ст.), в паровом и водогрейном котельном агрегате определяется по формулам:
Для парового котла
В н = (D Δi п) / (Q р р η бр),
Для водогрейного котла
В н = (G Δi в) / (Q р р η бр),
где D – паропроизводительность теплогенератора, кг/с; Δi п – прирост энтальпии пара и питательной воды, кДж/кг; Q р р – располагаемая теплота, кДж/кг, кДж/м 3 ; η бр – КПД брутто; G – расход воды через водогрейный котел, кг/с; Δi в – прирост энтальпии горячей и холодной воды, кДж/кг.
При сжигании газа и мазута, расчетный расход топлива В р равен натуральному расходу В н, так как потери теплоты от механической неполноты сгорания q 4 = 0.
Для увеличения ηбр необходимо снижать потери теплоты, а именно:
Работать по режимной карте, температурному графику, с наименьшим коэффициентом избытка воздуха: 1,05…1,1 – для природного газа; 1,1…1,15 – для мазута; 1,4…1,8 – для твердого топлива;
Следить за температурой уходящих топочных газов, полнотой сгорания топлива, обмуровкой котла.
5.3. Тепловые потери теплогенератора
Работа теплогенерирующей установки сопровождается потерями теплоты, выраженными обычно в долях, %:
q i = (Q i / Q р р) ⋅ 100.
1. Потери теплоты с уходящими топочными газами теплогенератора
q 2 = (Q 2 / Q р р) ⋅ 100, %.
В теплогенераторе это, чаще всего, наибольшая часть тепловых потерь. Потери теплоты с уходящими топочными газами можно понизить за счет:
Снижения объема дымовых топочных газов, путем поддержания требуемого коэффициента избытка воздуха в топке α т и уменьшения присосов воздуха;
Снижения температуры уходящих топочных газов, для чего применяют хвостовые поверхности нагрева: водяной экономайзер, воздухоподогреватель, контактный теплообменник.
Температура уходящих топочных газов (140…180 °С) считается рентабельной и во многом зависит от состояния внутренней и внешней поверхности нагрева труб котла, экономайзера. Отложение накипи на внутренней поверхности стенок труб котла, а также сажи (летучей золы) на внешней поверхности нагрева существенно ухудшают коэффициент теплопередачи от топочных газов к воде и пару. Увеличение поверхности экономайзера, воздухоподогревателя для более глубокого охлаждения дымовых газов не является целесообразным, так как при этом уменьшается температурный напор ΔТ и увеличивается металлоемкость.
Повышение температуры уходящих топочных газов может произойти в результате неправильного процесса эксплуатации и сжигания топлива: большой тяги (топливо догорает в кипятильном пучке); наличия неплотности в газовых перегородках (газы напрямую идут по газоходам котельного агрегата, не отдавая теплоты трубам – поверхностям нагрева), а также при большом гидравлическом сопротивлении внутри труб (за счет отложения накипи и шлама).
2. Химический недожог
q 3 = (Q 3 / Q р р) ⋅ 100, %.
Потери теплоты от химической неполноты сгорания топлива определяются по результатам анализа летучих горючих веществ Н 2 , СО, СН 4 в уходящих дымовых топочных газах. Причины химической неполноты сгорания: плохое смесеобразование, недостаток воздуха, низкая температура в топке.
3. Механический недожог
q 4 = (Q 4 / Q р р) ⋅ 100, %.
Потери теплоты от механической неполноты сгорания топлива характерны для твердого топлива и зависят от доли провала топлива через колосниковую решетку в систему шлакозолоудаления, уноса частичек несгоревшего топлива с дымовыми газами и шлаком, который может оплавить частицу твердого топлива и не дать ей полностью сгореть.
4. Потери теплоты от наружного охлаждения ограждающих конструкций
q 5 = (Q 5 / Q р р) ⋅ 100, %.
Возникают ввиду разности температуры наружной поверхности теплогенератора и окружающего наружного воздуха. Они зависят от качества изолирующих материалов, их толщины. Для поддержания q 5 в заданных пределах необходимо, чтобы температура наружной поверхности теплогенератора – его обмуровки не превышала 50 °С.
Потери теплоты q 5 уменьшаются по ходу движения топочных газов по газовому тракту, поэтому для теплогенератора введено понятие коэффициента сохранения теплоты
φ = 1 − 0,01q 5 .
5. Потери с физической теплотой шлака
q 6 = (Q 6 / Q р р) ⋅ 100, %.
Возникают за счет высокой температуры шлаков порядка 650 °С, и характерны только при сжигании твердого топлива.
Таблицы расчета тепловых потерь, коэффициента полезного действия брутто, натурального, расчетного и условного расхода топлива теплогенератора приведены в справочной литературе.
Лекция 4
6. Топочные и горелочные устройства
6.1. Топочные устройства
Топка – устройство, предназначенное для сжигания топлива с целью получения теплоты. Топка выполняет функцию горения и теплообменного аппарата – теплота одновременно передается от факела горения излучением и от продуктов сгорания конвекцией к экранным поверхностям, по которым циркулирует вода. Доля лучистого теплообмена в топке, где температура топочных газов порядка 1000 °С, больше чем конвективного, поэтому, чаще всего, поверхности нагрева в топке называют радиационными .
Для сжигания природного газа, мазута и пылевидного твердого топлива используются камерные топки, в конструкции которых можно выделить три основных элемента: топочную камеру, экранную поверхность, горелочное устройство.
1. Топочная камера или топочный объем – пространство, отделенное обмуровкой от окружающей среды.
Обмуровкой называют ограждения, отделяющие топочную камеру и газоходы теплогенератора от внешней среды. Обмуровку в котельном агрегате выполняют из красного или диатомового кирпича, огнеупорного материала или из металлических щитов с огнеупорами.
Внутренняя часть обмуровки топки – футеровка , со стороны топочных газов и шлаков, выполняется из огнеупорных материалов: шамотного кирпича, шамотобетона и других огнеупорных масс. Обмуровка и футеровка должны быть достаточно плотными, особо высокоогнеупорными, стойкими к химическому воздействию шлаков и иметь малый коэффициент теплопроводности.
Обмуровка может опираться непосредственно на фундамент, на металлические конструкции (каркас) или крепиться на трубах экранов топочной камеры и газоходов. Поэтому существуют три конструкции обмуровки: массивная – имеет свой фундамент; накаркасная (облегченная) – фундамента не имеет, крепится на металлический каркас; натрубная – крепится к экранным поверхностям.
Рис. 6.1. Фронтальный и боковой разрез водогрейного котла с топкой и обмуровкой из шамотного кирпича
Каркас служит для крепления и поддержания всех элементов котельного агрегата (барабанов, поверхностей нагрева, трубопроводов, обмуровки, лестниц и площадок) и представляет собой металлические конструкции обычно рамного типа, соединенные с помощью сварки или закрепленные болтами на фундаменте.
2. Экранная радиационная поверхность нагрева выполнена из стальных труб диаметром 51…76 мм, установленных с шагом 1,05…1,1. Экраны воспринимают теплоту за счет радиации и конвекции и передают ее воде или пароводяной смеси, циркулирующим по трубам. Экраны защищают обмуровку от мощных тепловых потоков.
В вертикально-водотрубных котлах (рис. 6.2а) поверхность нагрева состоит из развитого пучка кипятильных труб 2, ввальцованных в верхний 1 и нижний 3 барабаны, топочных экранов 6, питаемых водой из котельных барабанов через опускные трубы 7 и соединительные 4 из камер (коллекторов 5). Испарительные поверхности нагрева котельных агрегатов экранного типа (рис. 6.2б) состоят из барабана 1, системы экранных труб 6 с нижними 8 и 9 и верхними 5 экранными коллекторами, систем опускных 7 и соединительных 10 труб.
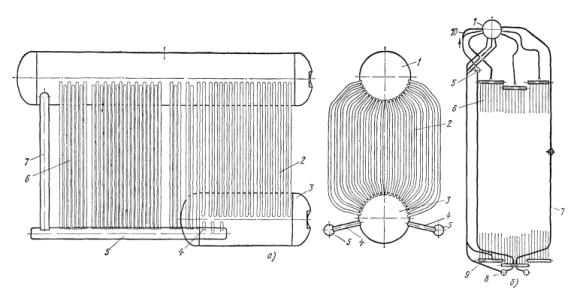
Рис. 6.2. Экранные поверхности нагрева котлов:
а – вертикально-водотрубных, б – экранного типа
1 и 3 – верхний и нижний барабаны, 2 и 7 – кипятильные и опускные трубы, 4 и 10 – соединительные трубы, 5, 8 и 9 – коллекторы, 6 – топочные экраны
3. Горелочные устройства устанавливаются на одной или двух противоположных (встречных) поверхностях нагрева, на поду, или в углах топки. На стенах топки котла устраивают амбразуру – отверстие в обмуровке, обмурованное огнеупорным материалом, куда устанавливают воздушный регистр и горелочное устройство.
При любом виде топлива (газообразное, жидкое или пылевидное) воздух в основном (кроме инжекционных горелок) нагнетается дутьевым вентилятором в топку через воздушные регистры или воздухонаправляющие аппараты, что обеспечивает интенсивное завихрение и выход (подачу) топливновоздушной смеси в наиболее узком сечении амбразуры топки со скоростью 25…30 м/с.
Воздухонаправляющее устройство представляет собой лопаточный завихритель осевого типа с подвижными, поворачивающимися вокруг своей оси лопатками. Возможна и установка неподвижных профильных лопаток под углом 45…50° к потоку воздуха. Завихрение потока воздуха интенсифицирует процессы смесеобразования и горения, но при этом увеличивается сопротивление по воздушному тракту. Направляющие аппараты удобны для автоматического регулирования производительности вентиляторов и дымососов.
6.2. Горелочные устройства
В зависимости от вида сжигаемого топлива различают множество конструкций горелочных устройств.
1. При сжигании твердого пылевидного топлива применяют горелки смешивающего типа. В амбразуре топочной камеры устанавливают улитку, в которой пылевоздушная смесь (пылевидное топливо с первичным воздухом) закручивается и по кольцевому каналу транспортируется к выходу горелки, откуда поступает в топку в виде закрученного короткого факела. Вторичный воздух, через другую аналогичную улитку, подается в топку со скоростью 18…30 м/с, в виде мощного закрученного потока, где интенсивно перемешивается с пылевоздушной смесью. Производительность горелок – 2…9 т/ч угольной пыли.
2. При сжигании мазута применяют форсунки и мазутные горелки: механические, ротационные и паровоздушные (паромеханические).
Механическая форсунка . Подогретый примерно до 100 °С мазут под давлением 2…4 МПа поступает в канал, перемещается в насадок (распыливающую головку), где установлен завихритель-распылитель.
Механические центробежные форсунки подразделяются на нерегулируемые и с регулируемым сливом. Следует отметить, что это деление весьма условное: можно изменять подачу у обеих форсунок. К нерегулируемым относят форсунки с малой глубиной регулирования и такие, у которых изменение подачи связано с их выключением, выемкой из топочного устройства и заменой распыливающего элемента.
Механические центробежные форсунки, различающиеся компоновкой распыливающих элементов, дополнительно иногда подразделяют на форсунки со сменными и постоянно работающими на всех режимах распылителями, что обусловлено в основном условиями эксплуатации котла.
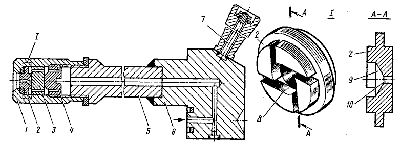
Рис. 6.3. Механическая нерегулируемая центробежная форсунка
Механическая регулируемая центробежная форсунка отечественных вспомогательных котлов (рис. 6.3) состоит из корпуса 6 с ручкой 7, ствола 5, представляющего собой толстостенную трубу со штуцером на конце, стопорной втулки 4, распределителя (сопла) 3, распыливающей шайбы 2 и головки 1. Топливо от топливно-форсуночного насоса по отверстиям в корпусе и каналу ствола через сверления в стопорной втулке и распределителе поступает к распыливающей шайбе. Распыливающая шайба у данной конструкции имеет четыре канала 8, расположенных тангенциально к окружности вихревой камеры. По ним топливо устремляется к центру и в вихревую камеру 9, где интенсивно раскручивается. Из нее топливо входит в топку через центральное отверстие 10 в виде вращающегося конуса мелко распыленных частиц.
Поверхности соприкосновения распыливающей шайбы 2 и распределителя 3 тщательно обрабатывают, полируют и при сборке головки прижимают одну к другой стопорной втулкой 4.
Распыливающие шайбы изготавливают из высоколегированных хромоникелевых или хромовольфрамовых сталей. В зависимости от подачи форсунки число тангенциальных каналов может быть от двух до семи.
Форма факела форсунки зависит от отношения f k /f o , в котором f k -суммарная площадь всех тангенциальных каналов, f o - площадь сечения центрального отверстия. Чем меньше это отношение, тем угол конуса распыливания будет больше, а длина факела меньше.
Шайбы изготавливаются обычно под номерами. Каждый номер соответствует определенной подаче, которая указывается в технической документации. Иногда на шайбах указываются числа, соответствующие значениям диаметра центрального отверстия и отношения f k /f o , при этом иностранные фирмы наносят условные обозначения в виде индексов (рис. 6.4). Например: буква X обозначает, что передняя торцевая стенка шайбы изготовлена плоской, буква W - сферической формы; цифра слева - условный номер сверла для изготовления центрального отверстия, цифра справа - отношение f k /f o , увеличенное в 10 раз.
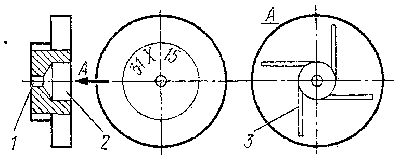
Рис. 6.4. Распыливающая шайба
Ротационная форсунка . Топливо подается через канал и сопло на вращающуюся чашу, дробится и сбрасывается в топочную камеру.
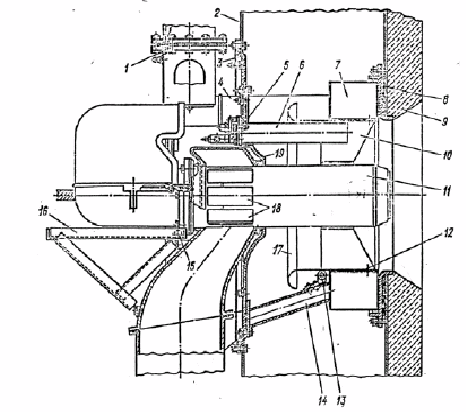
Рис. 6.5. Устройство ротационной газомазутной
горелки РГМГ-10 (-20, -30):
1 – газопровод; 2 – воздушный короб; 3 – кольцо рамы; 4 – газовая труба;
5 , 6 – труба установки запального защитного устройства (ЗЗУ) и фотодатчика; 7 – газовая камера; 8 – переднее кольцо воздухонаправляющего устройства; 9 – конический керамический туннель (амбразура); 10 – завихрители воздухонаправляющего устройства; 11 – ротационная форсунка;
12 – газовые выпускные отверстия; 13 – рамка для центровки завихрителя вторичного воздуха; 14 – опорная труба; 15 – подшипник направляющей рамы; 16 – направляющая рама; 17 – воздушный шибер; 18 – окно для подвода воздуха к завихрителю; 19 – крышка горелки
Давление топлива – мазута составляет 0,15…1 МПа, а чаша вращается со скоростью 1500…4500 об/мин. Воздух поступает вокруг чаши через конус, охватывает вращающийся поток капель и перемешивается с ним. Достоинства: не требуются мощные нефтенасосы и тонкая очистка мазута от примесей; широкий диапазон регулирования (15…100 %). Недостатки: сложная конструкция и повышенный уровень шума.
Паровоздушная или паромеханическая форсунка . Топливо подается в канал, по внешней поверхности которого поступает распыливающая среда – пар или сжатый воздух (давлением 0,5…2,5 МПа).
Пар выходит из канала со скоростью до 1000 м/с и распыливает топливо (мазут) на мельчайшие частички.
Воздух нагнетается вентилятором через амбразуру.
Котельные установки ...
Регистрационный номер ___209 тех/дс СТАНДАРТ
котельные установки , парогенераторы Котельные установки и парогенераторы котельных установок, их...
1 общая характеристика направления подготовки дипломир ованного специалиста по направлению « тепло энергетика»
Перечень образовательных программИ эксплуатация энергетических установок: котлы, котельные установки , парогенераторы , испарители, турбины, вспомогательное тепломеханическое... 240 СД.02 Котельные установки и парогенераторы : общая характеристика современных котельных установок, их...
Составители учебно-тематического плана программы повышения квалификации
ПрограммаМодуль 1 «Водоподготовка»; модуль 2 «Котельные установки и парогенераторы» ; модуль 3 «Паротурбинные установки ТЭС и АЭС»; модуль 4 « ... . ун-т, 2007. 65 с. Модуль 2. «Котельные установки и парогенераторы» Лабораторные работы 1. Раздел 2. Темы 2.1, 2.2, ...
Министерство образования и науки Российской Федерации
Федеральное агентство по образованию
Российский химико-технологический университет
имени Д.И. Менделеева
Е.М. Акимова, С.А. Першиков
Расчеты горения топлива.
Методические указания к выполнению курсового проекта
Москва 2006
Составители: Е.М. Акимова, С.А. Першиков
УДК 66.041.001.24(075)
БКК 24.54:34.35
Рецензент
Канд. техн. наук, доцент кафедры ХТКиО Российского химико-технологического университета им. Д.И. Менделеева
Ю.М. Мосин
Расчеты горения топлива. Методические указания к выполнению курсового проекта/ Сост. Е.М. Акимова, С.А. Першиков. – М.: РХТУ им. Д.И. Менделеева, 2006. – 28 с.
УДК 66.041.001.24(075)
БКК 24.54:34.35
© Российский химико-технологического университет им. Д.И. Менделеева
© Е.М. Акимова, С.А. Першиков
Введение
Расчеты горения топлива производят для определения необходимого для горения расхода воздуха, количества дымовых газов, их состава и температуры. Если данное топливо не обеспечивает необходимые температуры в печи, то рассчитывают температуру подогрева воздуха, участвующего в горении. Расход воздуха на горение и объем дымовых газов в этих расчетах отнесены к единице массы (1 кг) твердого или жидкого топлива или к единице объема (1 нм 3) газообразного топлива, т.е. являются удельными величинами.
Выбор топлива
При проектировании промышленного предприятия выбор топлива для тепловых агрегатов производят на основе технико-экономических расчетов.
Твердое топливо обычно используют для отопления печей как дешевое местное топливо и только при условии, что обрабатываемый материал (например, цементный клинкер) допускает загрязнение негорючей золой.
Жидкое топливо обладает наиболее высокой теплотворной способностью по сравнению с другими видами, оно – самое дорогое и рассматривается в настоящее время как вспомогательное (резервное) топливо.
Природный газ различных месторождений сочетает высокую теплотворную способность с умеренной ценой и отсутствием золы. Его применение целесообразно в любых тепловых агрегатах. Однако газ дает прозрачное пламя, которое излучает тепло менее интенсивно, чем пламя от сжигания угольной пыли или мазута.
Пересчеты составов топлива
Основой расчетов горения топлива является его состав. В горении участвует только часть топлива, которая называется горючей массой . Непосредственно на горение поступаетрабочее топливо , которое содержит помимо горючей массы влагу, а твердое и жидкое топливо – золу.
Состав топлива для выполнения расчетов может быть взят по результатам анализа или из справочника (см. Приложение, табл. 1–3). Однако необходимо учитывать, что для газообразных топлив состав приводится на сухой газ (включая негорючие компоненты), для твердых и жидких топлив – на горючую массу, реже на рабочее топливо.
Обычно, зная состав горючей массы топлива и принимая по данным анализа или по справочнику содержание золы (А с , %) в сухом топливе и влаги (W р , %) в рабочем топливе, пересчитывают все топливо на рабочую массу.
|
А
р
= А
с
|
|
С
р
= С
г
|
где С р – содержание отдельной составляющей рабочей массы топлива, % (здесь – углерод),С г – содержание той же составляющей горючей массы топлива, %.
Сухое газообразное топливо пересчитывают на влажный газ, который подлежит сжиганию. В природном газе содержится небольшое количество влаги, примерно 0,5÷1,5%, так как при транспортировании газа он подвергается очистке от примесей и большей части влаги.
Часто сумма процентных содержаний компонентов сухого газообразного топлива не равна 100%. Тогда содержание каждого компонента во влажном рабочем газе, например СН 4 вл, рассчитывают по формуле:
где
 – сумма концентраций компонентов сухого
топлива (без учета содержания Н 2 О).
– сумма концентраций компонентов сухого
топлива (без учета содержания Н 2 О).
(Реферат)
n1.doc
Топливо и его горение 2
Химический состав топлива. 2
Элементарный анализ топлива. 2
Теплота сгорания топлива. 3
Условное топливо. 3
Газообразное топливо. 4
Жидкое топливо. 4
Твердое топливо. 4
Горение топлива. 5
Горение газообразного топлива. 5
Горение жидкого топлива. 6
Горение твердого топлива. 6
Расчет горения топлива. 7
Расчет горения смеси природного и доменного газов. 9
Исходные данные для расчета 9
Расчет состава природно-доменной смеси. 9
Список использованной литературы 15
Топливо и его горение
Основным источником энергии для металлургической промышленности является топливо.Под топливом понимают вещество, горение которого сопровождается выделением значительного количества тепла и которое отвечает следующим требованиям:
запасы должны быть достаточными для того, чтобы их было экономически выгодно добывать и попользовать;
продукты сгорания должны легко удаляться из зоны горения;
продукты сгорания должны быть безвредны для окружающего мира и самих тепловых устройств;
процесс горения должен быть легко управляем.
Все виды топлива подразделяют на естественное и искусственное, каждое из которых в свою очередь подразделяются на твердое, жидкое, газообразное.
Химический состав топлива.
Топливо состоят из горючей массы и балласта. К горючим компонентам относятся С, Н, S (сера органическая и колчеданная). В состав топлива входят азот N (не горит, теплоноситель), кислород О (окисляет горючие компоненты).Кроме этого в топливе всегда присутствуют вода и зола. Вода, содержащаяся в топливе, подразделяется на гигроскопическую, химически связанную и внешнюю, которая механически удерживается в топливе и теряется при сушке.
Зола – это негорючая минеральная часть топлива, состоящая из Al 2 O 3 , Fe 2 O 3 , Si 2 O 3 , CaO и др.
Элементарный анализ топлива.
| Индекс | Состав |
||||||
| C | H | O | N | S | A | W |
|
| О | органическая масса | ||||||
| Г | горючая масса | ||||||
| С | сухая масса | ||||||
| Р | рабочая масса |
||||||
Состав рабочего топлива:
С Р + H Р + O Р + N Р + S Р + A Р + W Р = 100%
Пересчет состава топлива с любой массы на рабочее топливо выполняется по одному из следующих выражений:
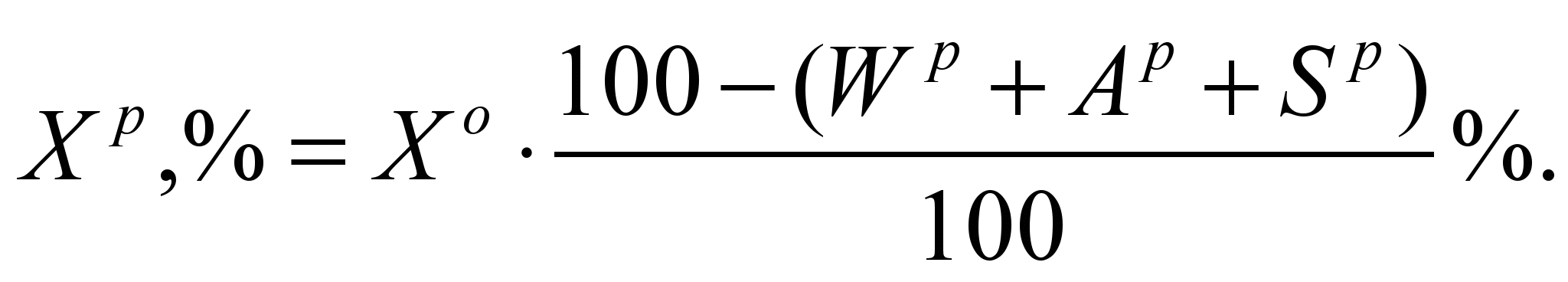
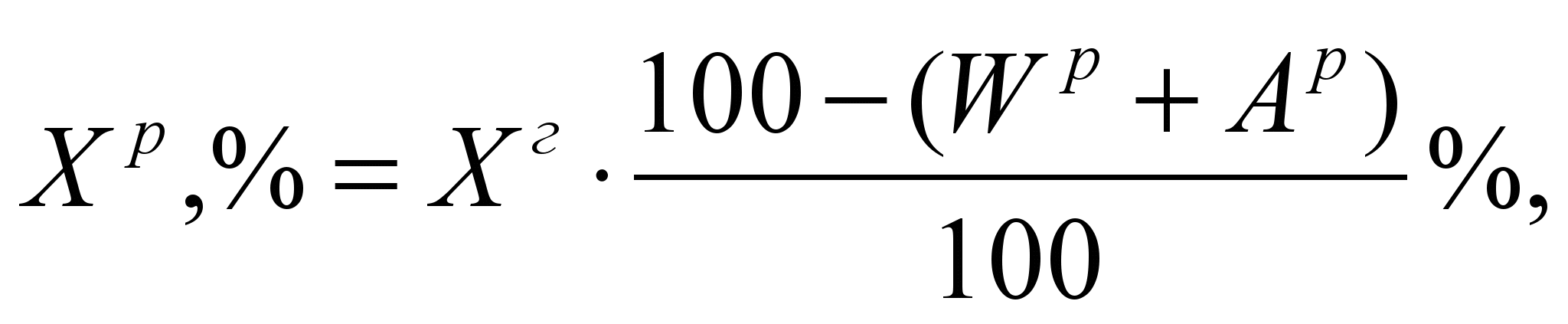
Теплота сгорания топлива.
Количество выделившегося тепла при сжигании топлива связано с химическим составом топлива.Количество тепла, которое выделяется при сжигании единицы топлива, называется теплотой сгорания топлива Q. Ее размерности: кДж/кг (ккал/кг), кДж/м 3 (ккал/м 3) или кДж/кмоль (ккал/кмоль).
В технике различают высшую Q в и низшую Q н теплоту сгорания топлива. Под низшей теплотой сгорания понимают то количество тепла, которое выделяется при сжигании единицы топлива до продуктов полного сжигания при условии, что вода, содержащаяся в продуктах сгорания, находится в виде пара, охлажденного до 20 о С.
Теплота сгорания топлива определяется по следующим формулам:
Для твердого и жидкого топлива:
для газообразного:
,
где C P , H P , CO, H 2 и т.д. – составляющие топлив, %;
4, 187кДж = 1ккал.
Условное топливо.
Для удобства планирования, учета и сравнения различных видов топлива введено понятие условного топлива, которое характеризуется низшей теплотой сгорания.
Для перевода натурального топлива в условное находится эквивалент данного топлива:
Для твердого и жидкого:
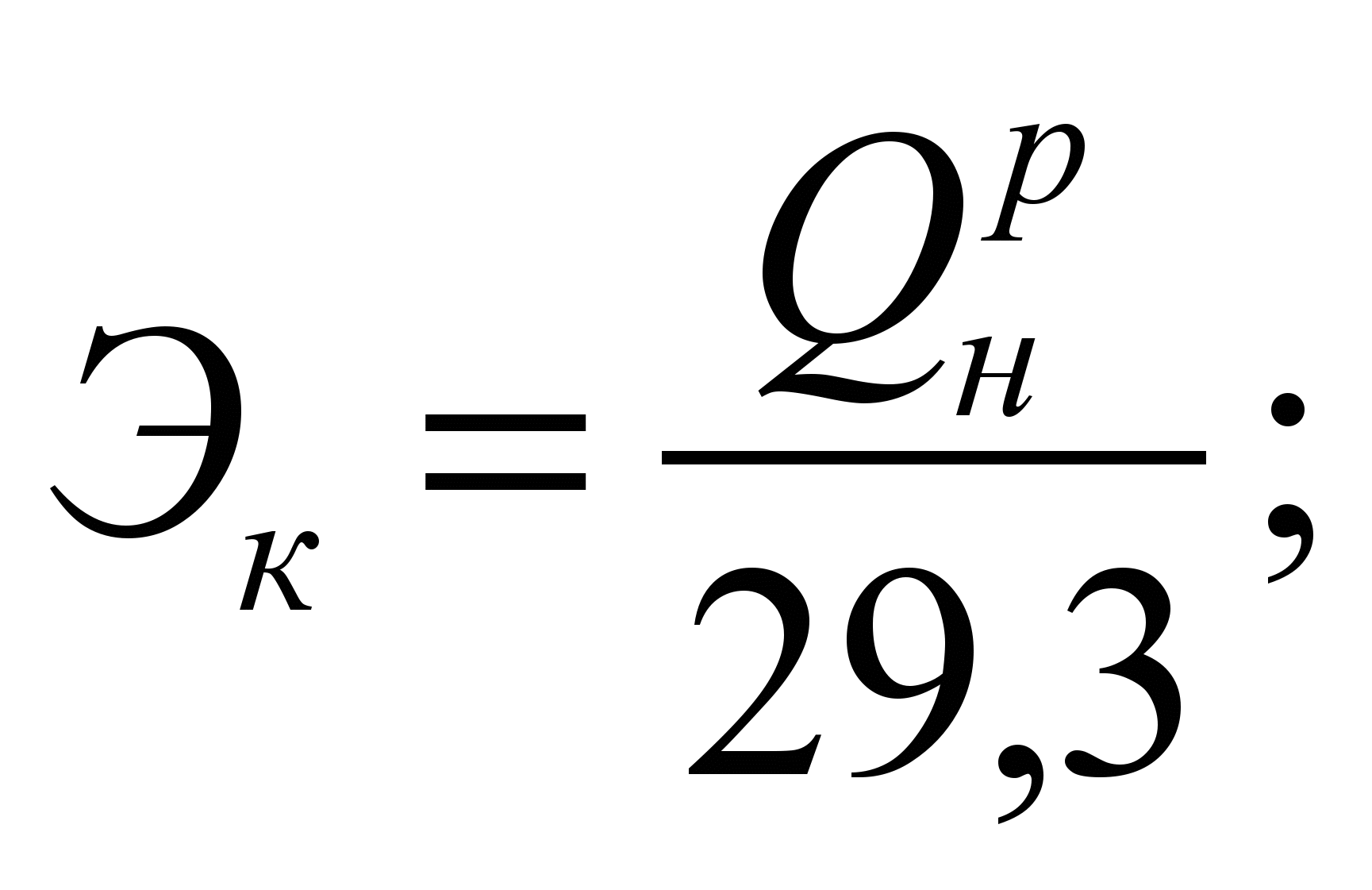
Для газообразного:
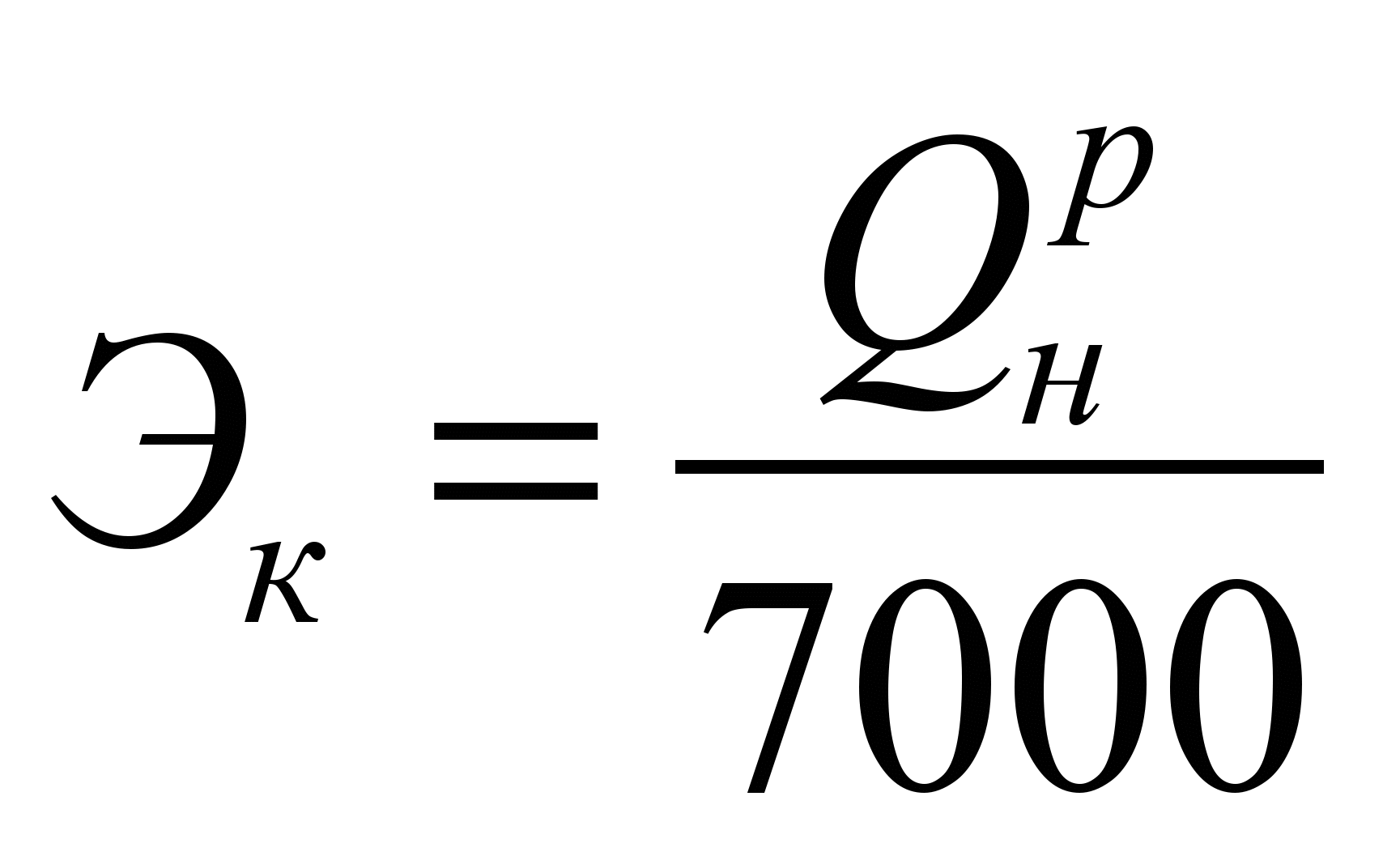 .
.
Перерасчет расхода натурального топлива Вр на условное Ву осуществляется по формуле: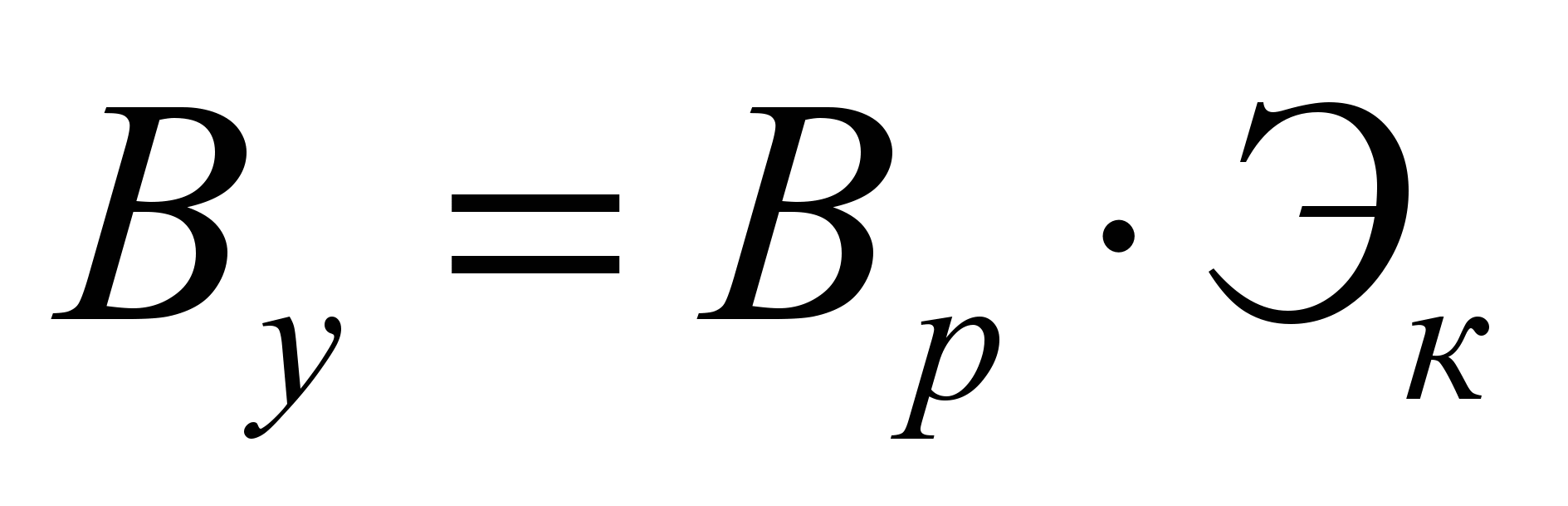
Газообразное топливо.
Газообразное топливо по сравнению с твердым и жидким топливом обладает следующими преимуществами:
возможностью лучшего смешения газа с воздухом и, следовательно, сжиганием с меньшим избытком воздуха;
легкостью подогрева перед сжиганием;
отсутствием золы;
транспортабельностью и удобством учета расхода газа;
простотой обслуживания горелочных устройств.
Природный газ – наиболее дешевое топливо. Его основным горючим компонентом является метан CH 4 = 95%.
Искусственные газы:
коксовый газ – продукт коксования углей;
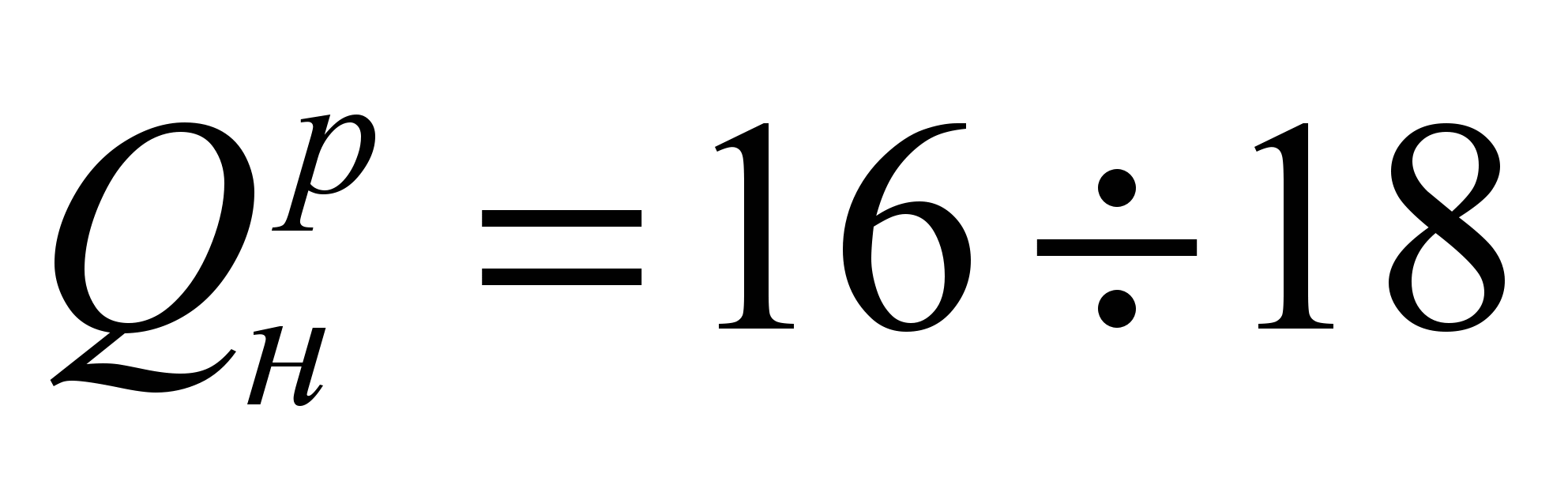 МДж/м 3 ;
МДж/м 3 ;Жидкое топливо.
Естественное жидкое топливо – нефть. Как топливо ее используют редко.Искусственное жидкое топливо – это продукты переработки нефти: бензин, лигроин, керосин, газойль и др. Остаток переработки – мазут. Мазут – топливо металлургической промышленности и энергетики. Перед сжиганием мазут нагревают до 70-80 о С с целью понижения его вязкости. Состав мазута – это соединения углеродов. С = 85-88%; Н 2 = 10%; 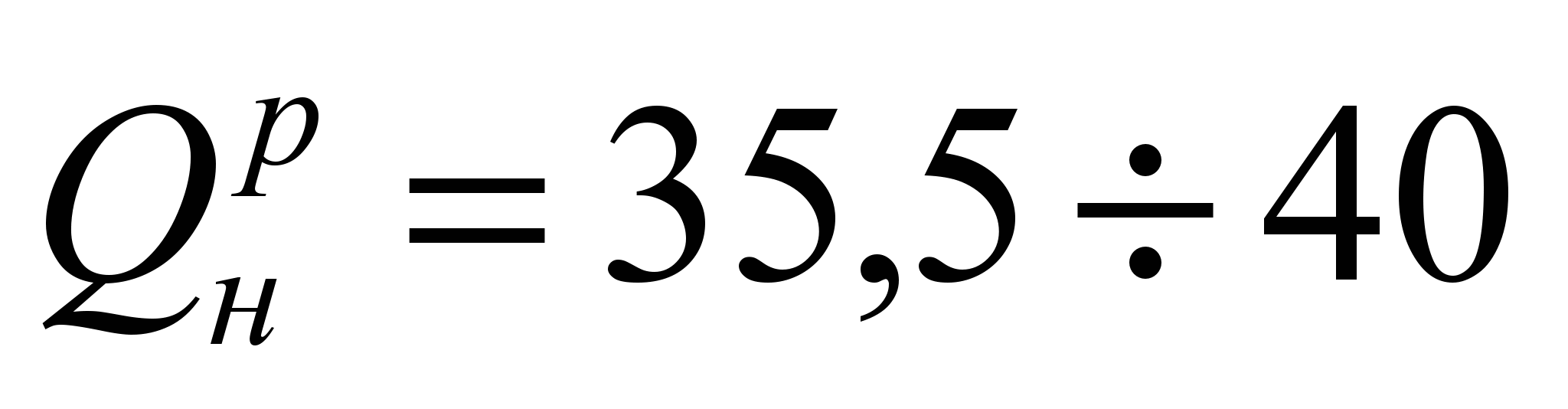 МДж/кг.
МДж/кг.
Твердое топливо.
Это каменный и бурый угли, антрацит, горючие сланцы, торф.Основной метод переработки угля – коксование, заключающийся в сухой перегонке топлива путем нагрева угля без доступа воздуха при температурах 900-1100 о С в коксовых печах. Получается спекшийся кокс, пористый, механически прочный, применяемый в металлургии, в основном для выплавки чугуна. Содержание С=75-85%; 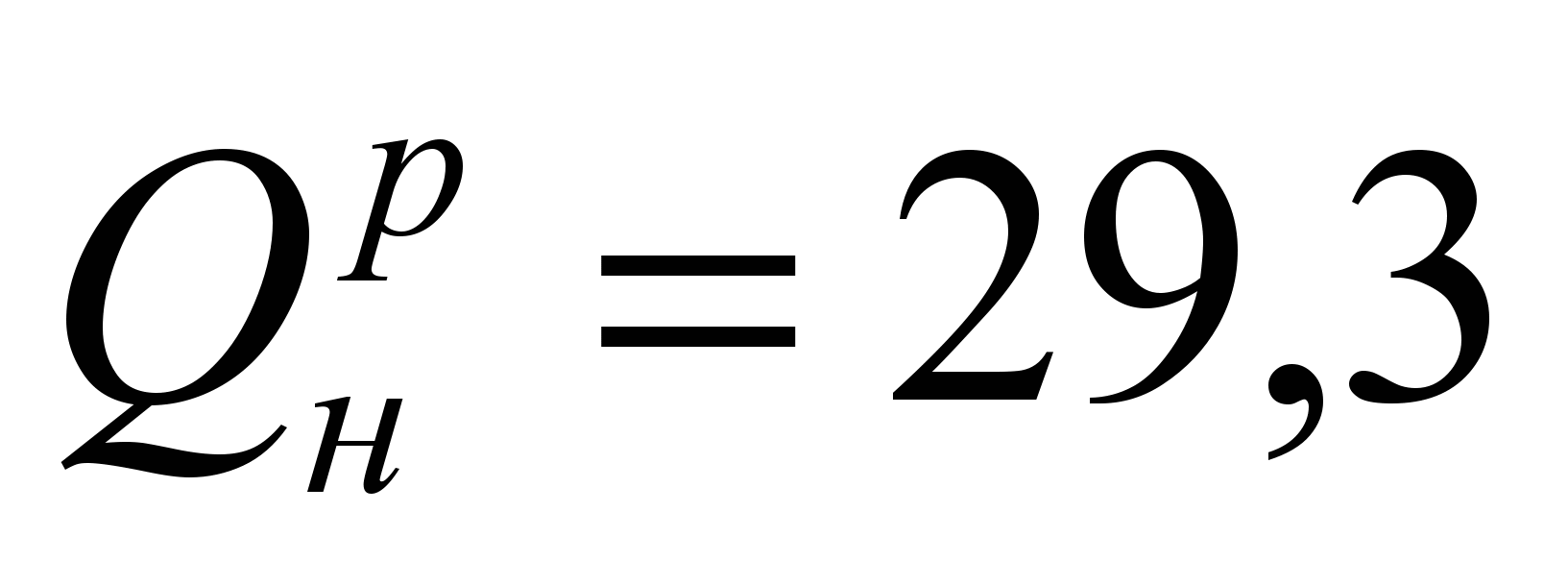 МДж/кг.
МДж/кг.
Горение топлива.
Горением называют химический процесс соединения топлива с окислителем, сопровождающийся интенсивным тепловыделением и быстрым подъемом температуры продуктов сгорания.Объем движущихся газов, в котором совершаются процессы горения, называется пламенем.
В зависимости от величины коэффициента расхода n (отношение действительного расхода к теоретическому), условий смешения окислителя и топлива, горение топлива бывает полное или неполное.
Полное горение топлива получается при n ? 1 и полном смешении топлива с окислителем.
Неполное горение:
химический недожог получается при n ? 1;
механический недожог получается при n ? 1 из-за плохого смешения окислителя с топливом, кроме того, унос частиц с газом, провалом твердого топлива сквозь колосниковую решетку.
Следует помнить, что основную роль для обеспечения полного сжигания топлива при n ? 1 играет стадия смешения топлива с окислителем.
Горение газообразного топлива.
Процесс горения любого топлива разделяется на две стадии: воспламенение и непосредственное горение.Полное сгорание основных горючих составляющих газообразных топлив происходит по следующим реакциям:
CH 4 + 2O 2 = CO 2 + 2H 2 O + 8580ккал/нм 3 ;
H 2 + ЅO 2 = H 2 O + 2580ккал/нм 3 ;
CO + ЅO 2 = CO 2 + 3022ккал/нм 3 .
Неполное горение метана:
СН 4 + ЅО 2 = СО + 2Н 2 + 396ккал/нм 3 .
Горение газообразного топлива бывает кинетическое и диффузорное:
под кинетическим горением понимают горение газовой смеси горючего и окислителя; в этом случае полное время процесса определяется только скоростью химической реакции;
при диффузорном горении процессы смешения и горения происходят в одном объеме; лимитирующим процессом является процесс смешения – физический процесс, протекающий с меньшей скоростью, чем собственно процесс горения.
Горение жидкого топлива.
В условиях промышленных печей жидкое топливо (обычно мазут) сжигают в распыленном состоянии. Кинетика горения: жидкое топливо, распыленное до мелких капель, попадая в пространство печи, нагретое выше температуры самовоспламенения, начинает испаряться, дальше смешивается с окислителем и горит.Горение твердого топлива.
Процесс горения твердого топлива может быть разделен на следующие стадии:
подогрев и подсушка топлива;
процесс пирогенного разложения топлива с выделением летучих и образованием коксового остатка;
горение летучих, горение коксового остатка (углерод).
С + О 2 = СО 2 + 7980ккал/(кг о С);
Неполное горение углерода:
2С + О 2 = 2СО + 2340ккал/(кг о С).
Расчет горения топлива.
Для удобства расчет горения твердого и жидкого топлива ведется на 100кг топлива, а расчет горения газообразного топлива на 100м 3 .При расчете делают следующие допущения:
смешение окислителя с горючим идеальное, и горение идет до полного сгорания топлива (до СО 2 и Н 2 О);
в системе достигнуто термодинамическое равновесие;
диссоциация продуктов сгорания и горючих принимается равной нулю.
Целью расчета является определение:
количества необходимого для горения воздуха или дутья, обогащенного кислорода.
Действительный расход L д для более полного сжигания обычно теоретический L т, т.к. в реальных условиях газогорелочными устройствами не обеспечивается идеальное смешение.
Отношение 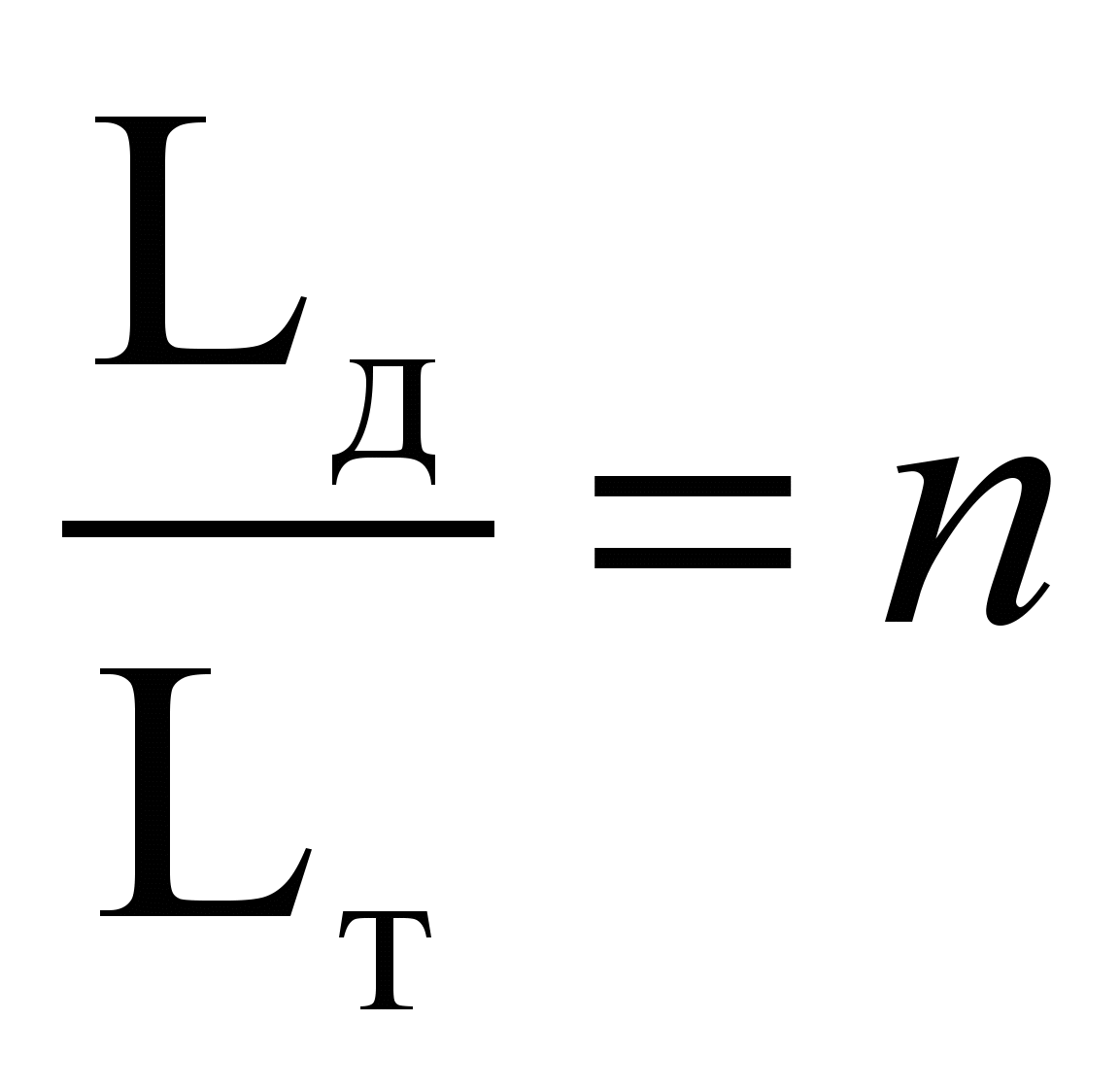 называется коэффициентом расхода воздуха.
называется коэффициентом расхода воздуха.
количества состава и плотности образующихся продуктов сгорания.
температуры горения.
действительная температура – это та температура, которую имеют продукты сгорания в конкретных условиях процесса сжигания топлива, она определяется по формуле:
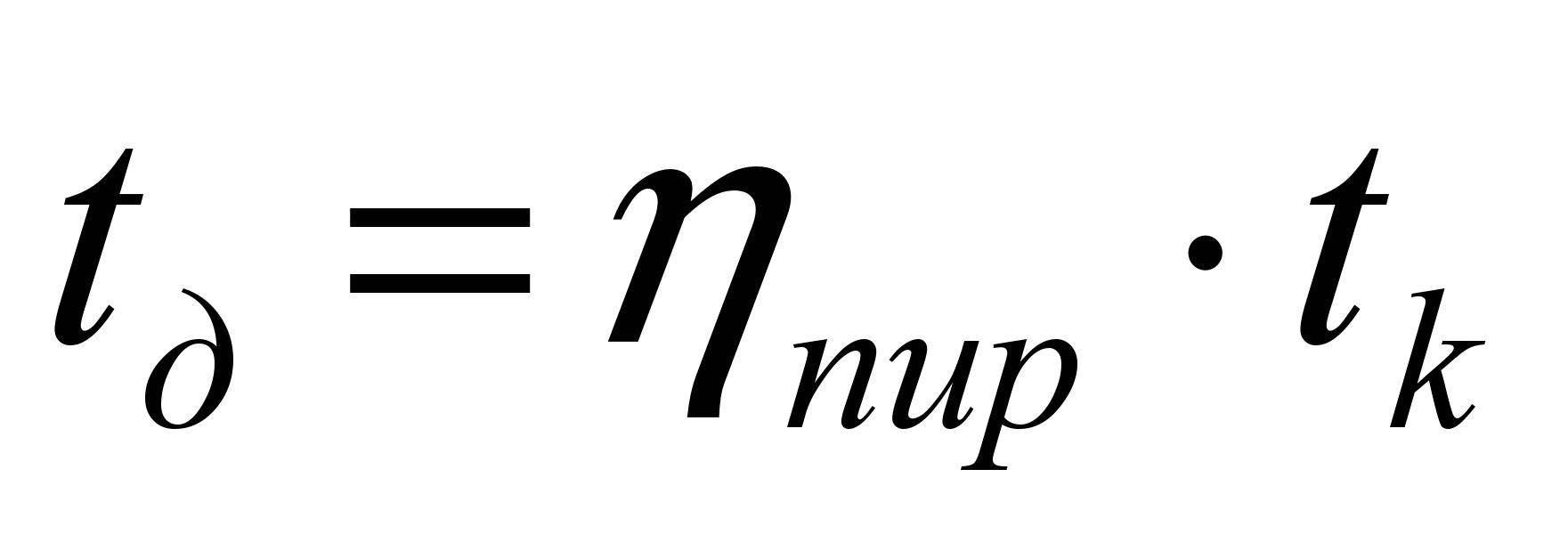 ,
,
где 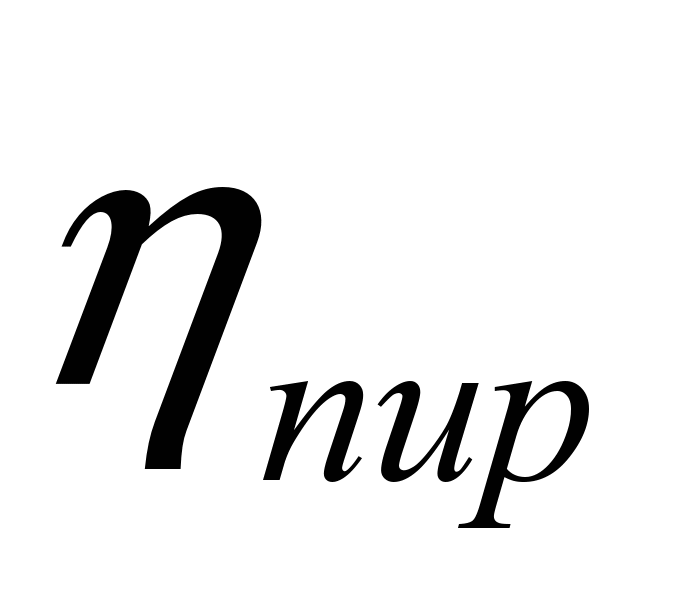 – пирометрический коэффициент (определяется экспериментально);
– пирометрический коэффициент (определяется экспериментально);
Для топочных камер = 0,95;
Для мартеновских печей = 0,85-0,9;
Для садочных печей = 0,8-0,85;
Для проходных и протяжных = 0,7-0,75;
T k – калориметрическая температура горения, о С.
теоретическая температура горения определяется с учетом диссоциации в продуктах сгорания:
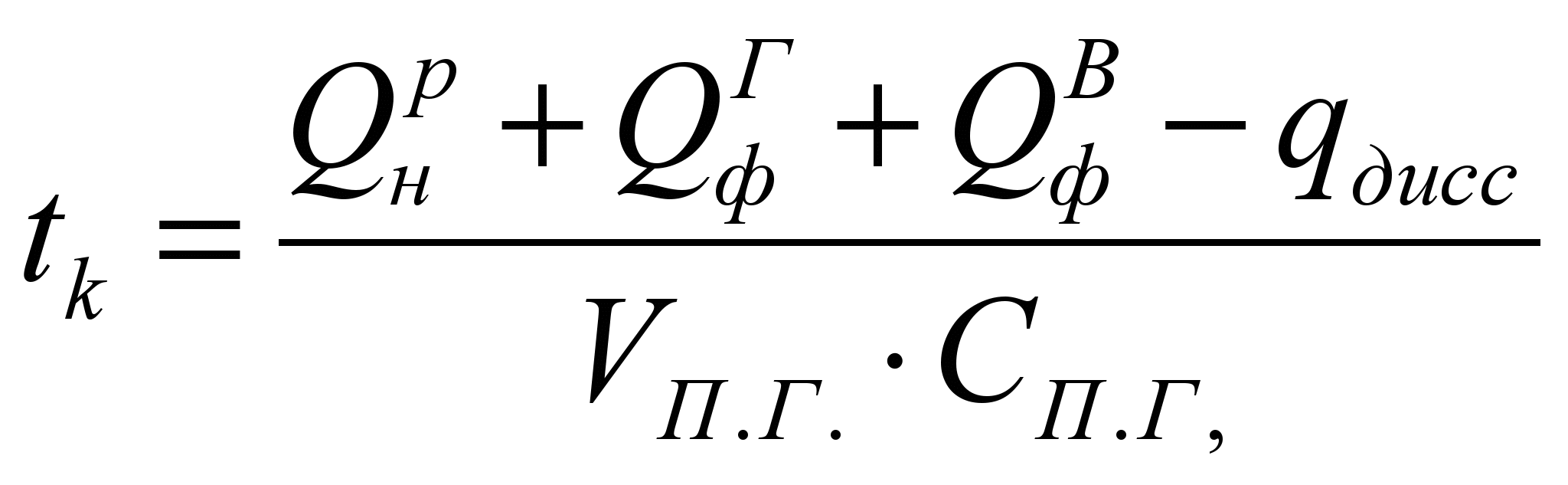 ,
,
где 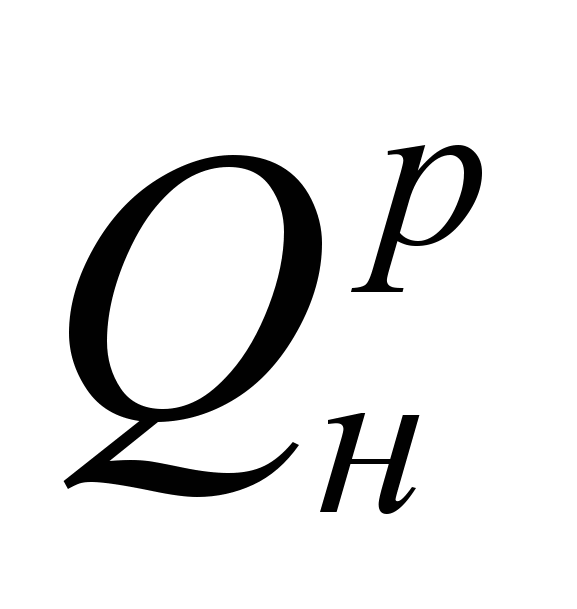 – теплота сгорания топлива, кДж/м 3 или кДж/кг;
– теплота сгорания топлива, кДж/м 3 или кДж/кг;
Q дисс – тепло, пошедшее на процесс диссоциации, кДж;
V П.Г. – объем продуктов сгорания, образующихся при сгорании единицы топлива, м 3 ;
С П.Г. – объемная теплоемкость продуктов сгорания, кДж/(м 3 о С).
калориметрическая температура определяется из условия, что все выделившееся при горении тепло расходуется на повышении температуры продуктов сгорания (т.е. для адиабатных условий):
,
где 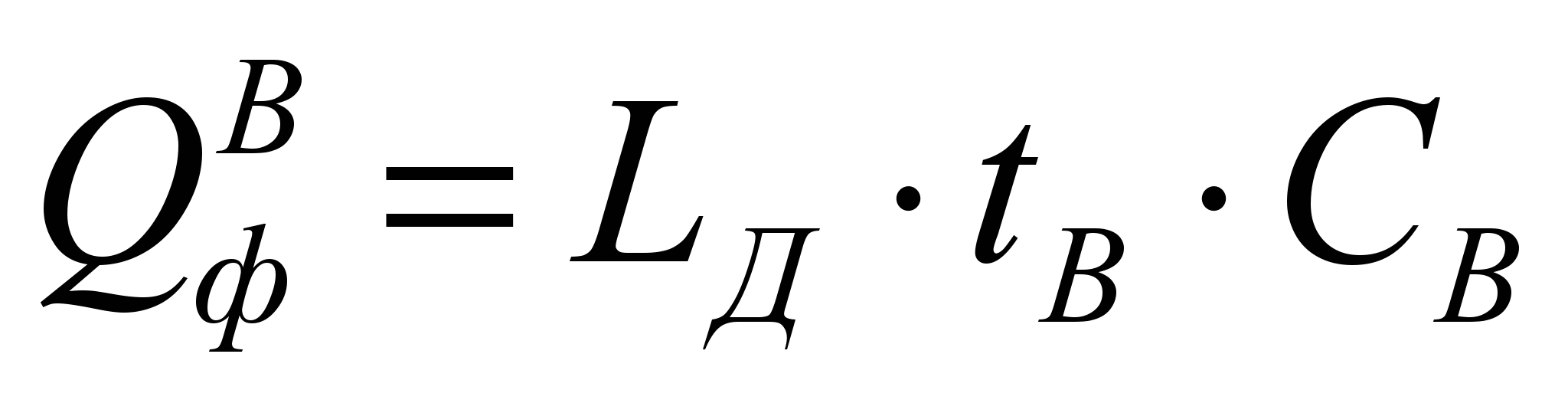 – физическое тепло подогретого воздуха, кДж/м 3 или кДж/кг;
– физическое тепло подогретого воздуха, кДж/м 3 или кДж/кг;
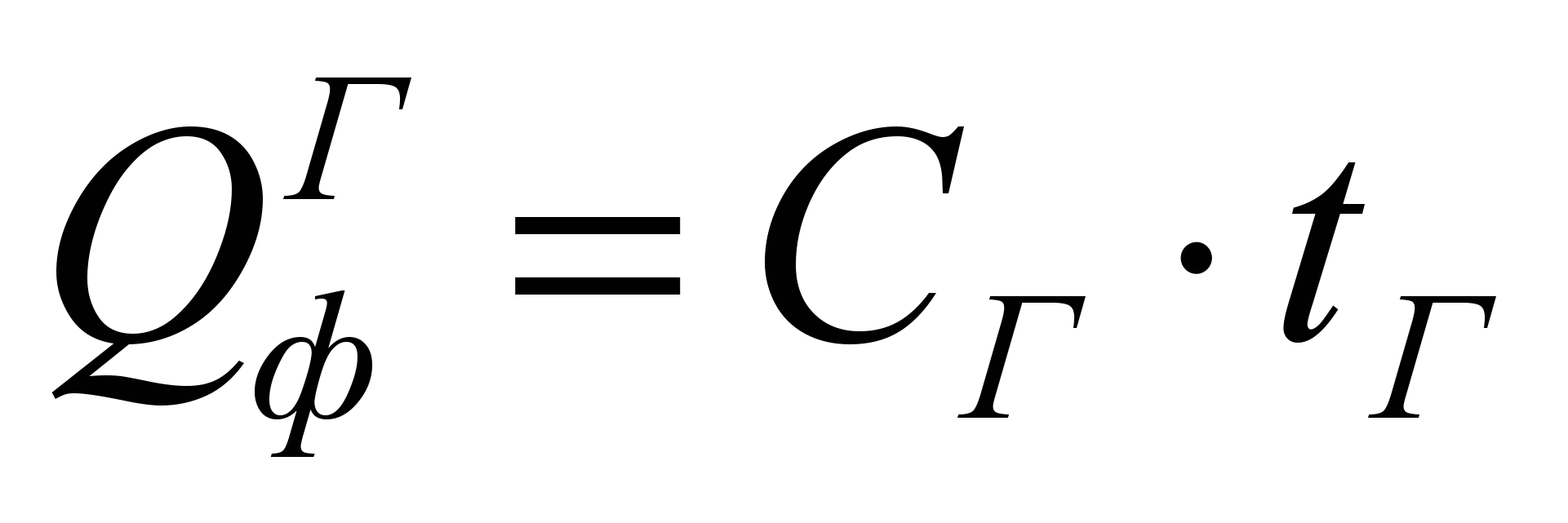 – физическое тепло подогретого топлива. кДж/м 3 или кДж/кг;
– физическое тепло подогретого топлива. кДж/м 3 или кДж/кг;
L д – объем воздуха на единицу топлива, м 3 /м 3 или м 3 /кг;
С В и С Г – средние теплоемкости воздуха и топлива, кДж/(м 3 о С).
Калориметрическую температуру находим методом последовательных приближений, используя понятие энтальпии.
Начальная энтальпия продуктов сгорания определяется по формуле: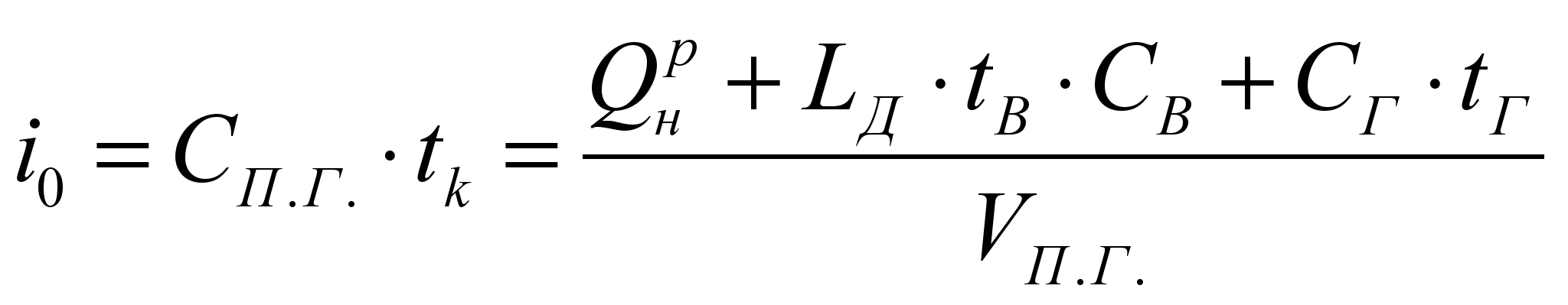 ,
,
По значению 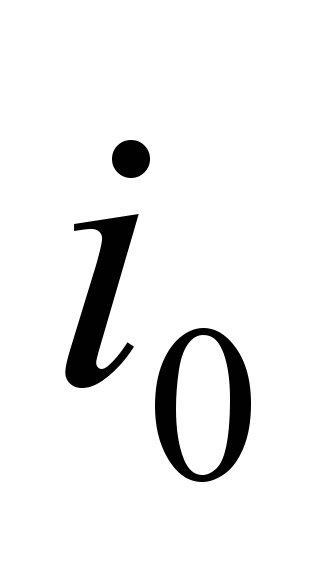 задаемся возможным значением температуры горения 1 и при этой температуре находим энтальпию продуктов сгорания. Если
задаемся возможным значением температуры горения 1 и при этой температуре находим энтальпию продуктов сгорания. Если 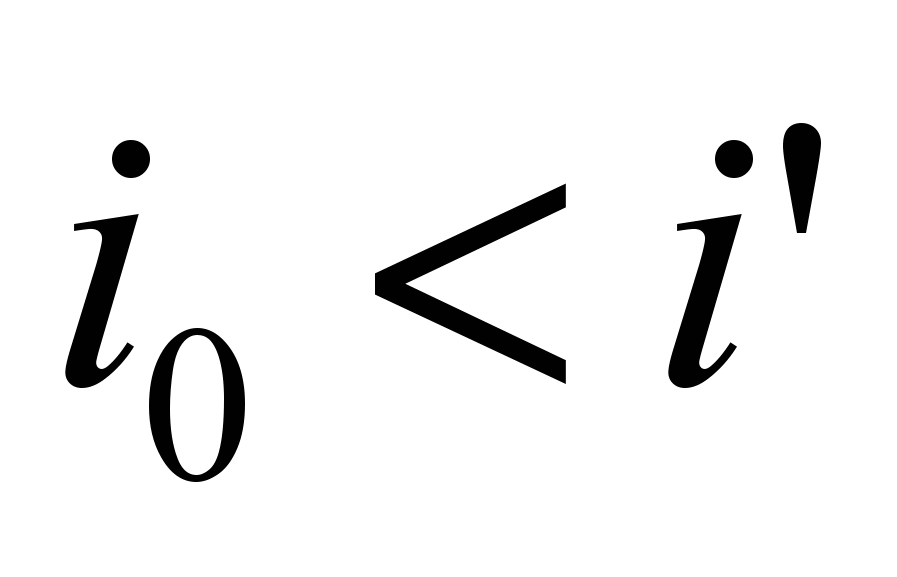 , то истинная калориметрическая температура ниже, чем
, то истинная калориметрическая температура ниже, чем 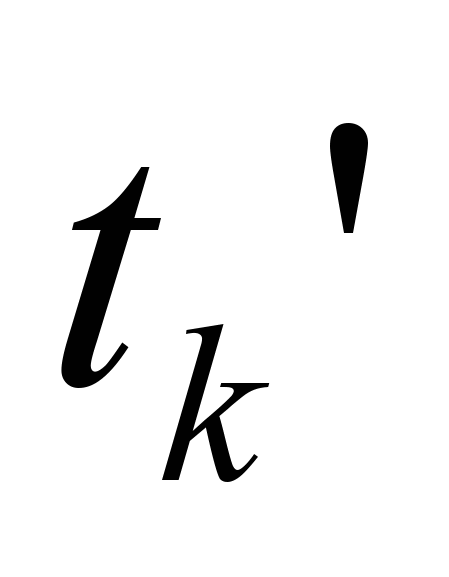 . Поэтому задаемся температурой
. Поэтому задаемся температурой 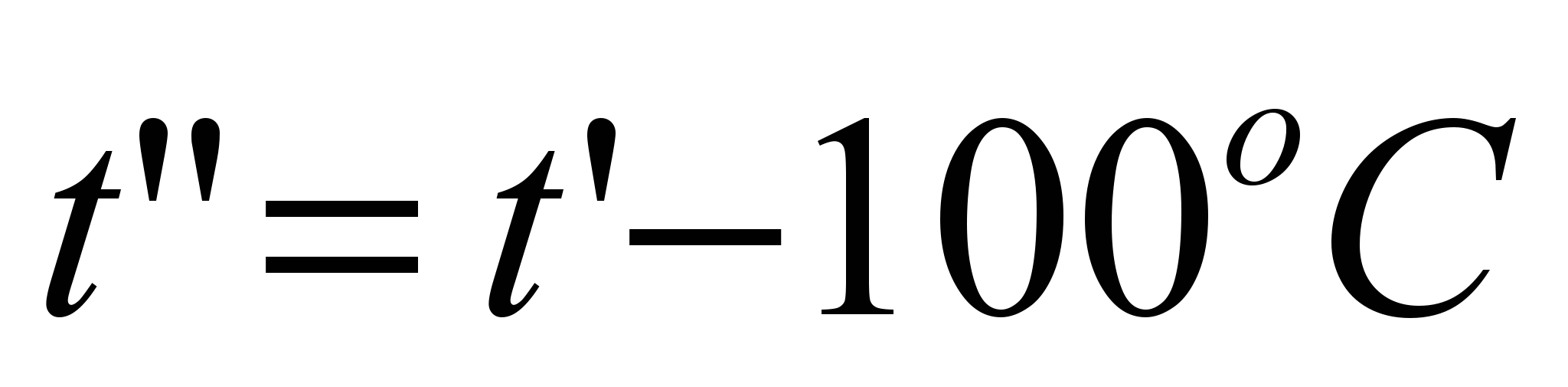 и снова находим энтальпию продуктов сгорания. Если
и снова находим энтальпию продуктов сгорания. Если 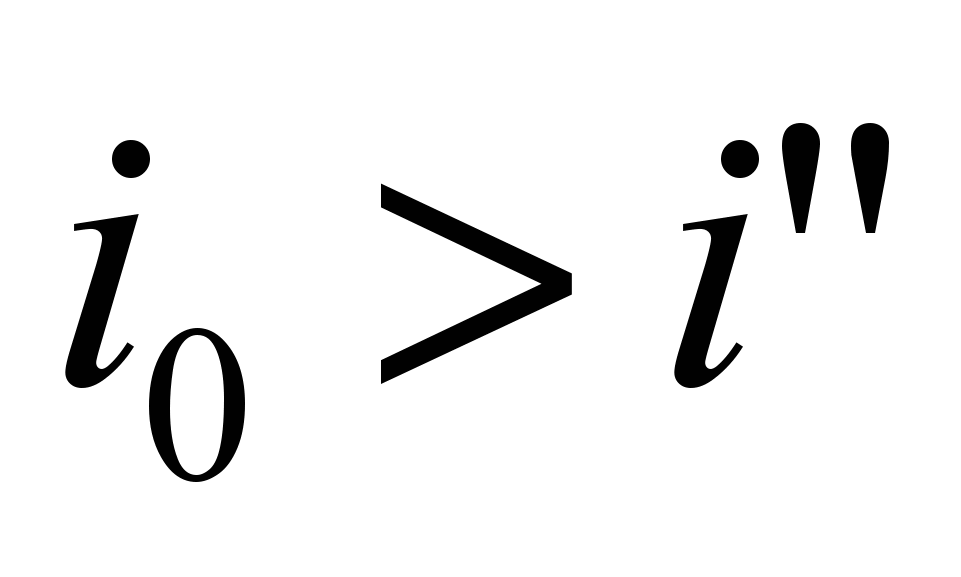 , то действительная калориметрическая температура продуктов сгорания лежит в интервале
, то действительная калориметрическая температура продуктов сгорания лежит в интервале 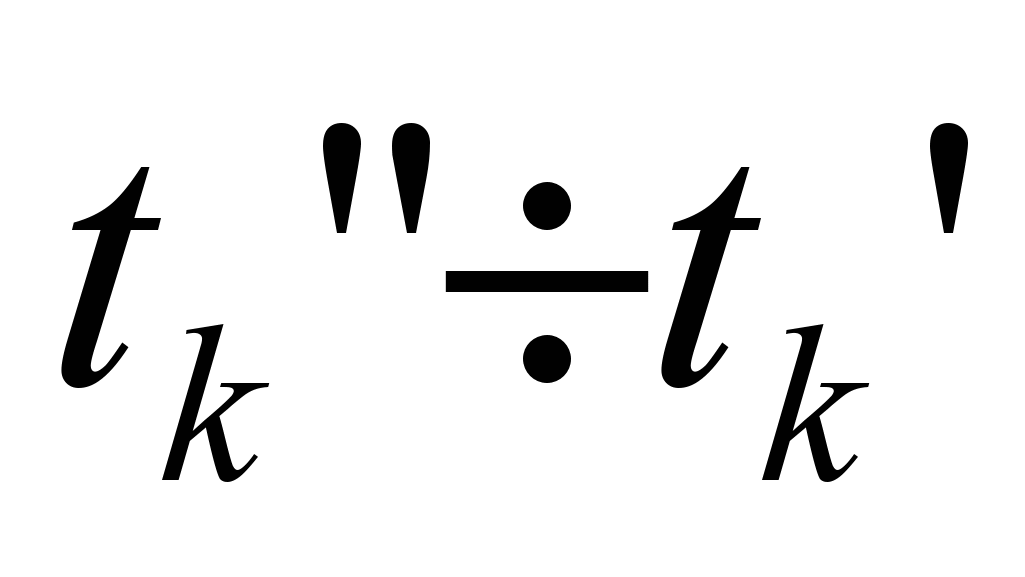 и может быть найдена по формуле:
и может быть найдена по формуле: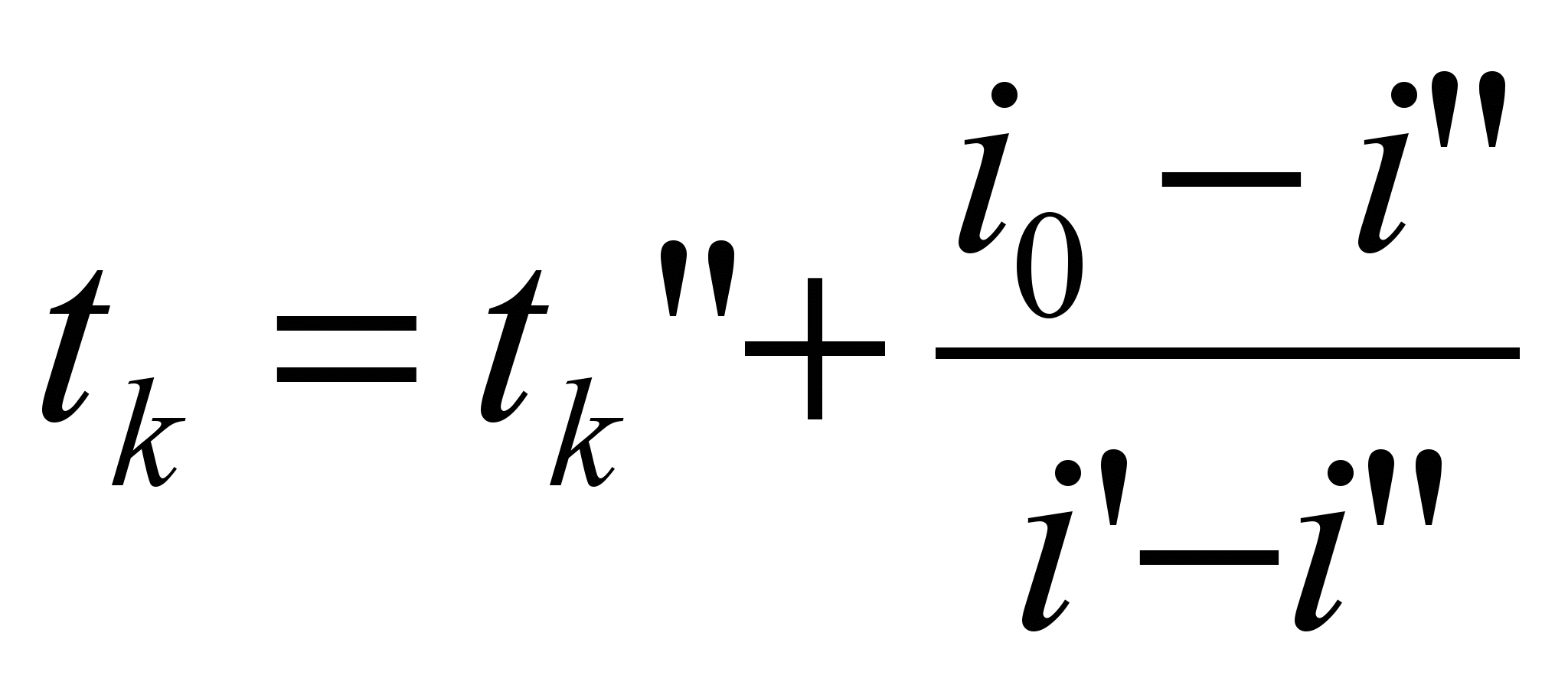 .
.
Окончательное значение t k следует перевести в градусы Кельвина.
Расчет горения смеси природного и доменного газов.
Исходные данные для расчета
t Г = 400 о С = 673К;
Температура уходящих продуктов сгорания (дыма): t П.Г. = 840 о С = 1113К;
Расчет ведется на 1м 3 газа.
Расчет состава природно-доменной смеси.
1. Пересчет состава сухого доменного газа на влажный.Объемный процент водяных паров во влажном доменном газе:
.
Коэффициент пересчета состава сухого доменного газа во влажный (рабочий):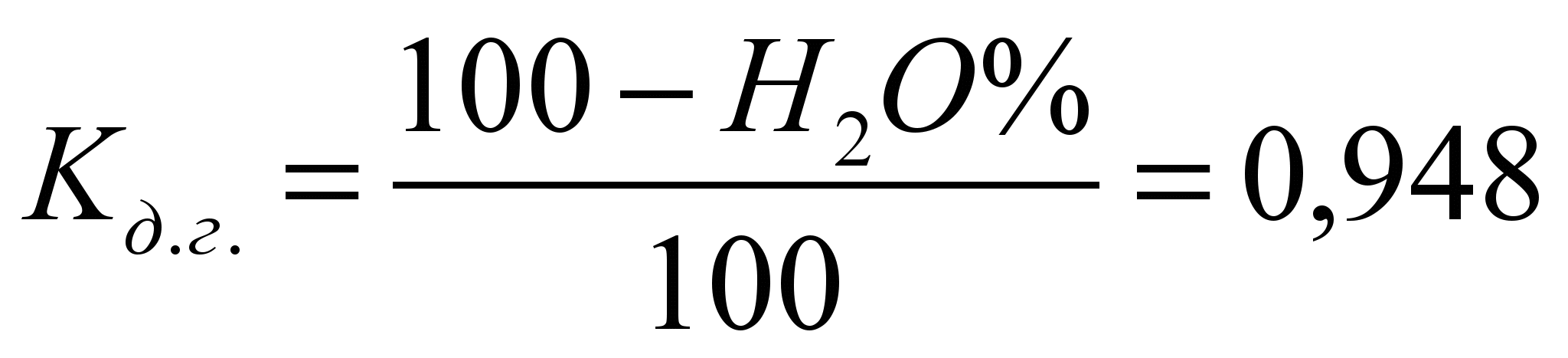 .
.
Рабочий состав доменного газа:
;
.
Таблица 1. Состав рабочего доменного газа.
| Газ | СН 4 | СО 2 | H 2 | CO | N 2 | H 2 O | ? |
| Доменный | 0,285 | 12,039 | 1,337 | 25,596 | 55,553 | 5,19 | 100 |
2. Определение теплоты сгорания газов .
Природного газа:
.
Доменного газа:
.
3. Расчет состава смеси природного и доменного газов.
Принимаем долю доменного газа в природно-доменной смеси (ПДС) за x, тогда доля природного газа будет равна y = (1-x). Составляем уравнение:
,
где 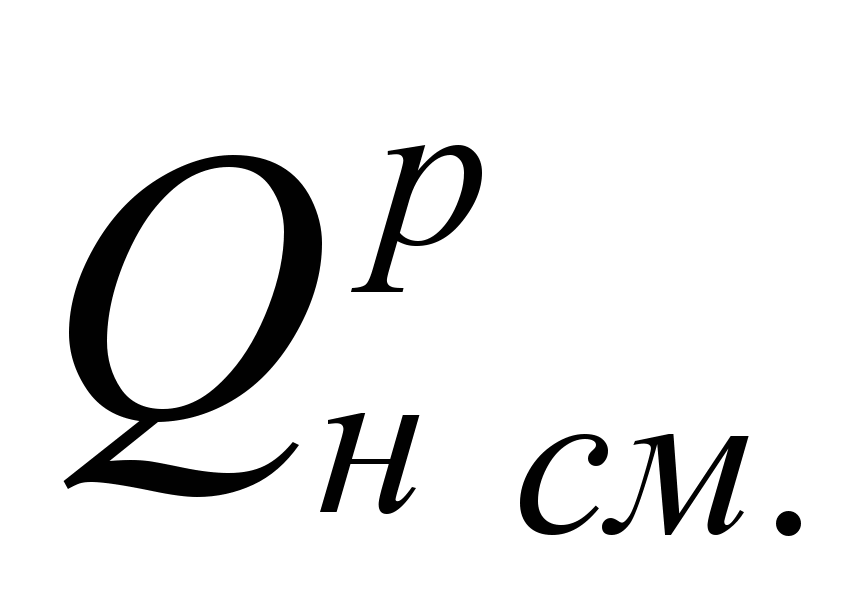 – исходная теплота сгорания смеси газов, МДж/м 3 .
– исходная теплота сгорания смеси газов, МДж/м 3 .
Находим, что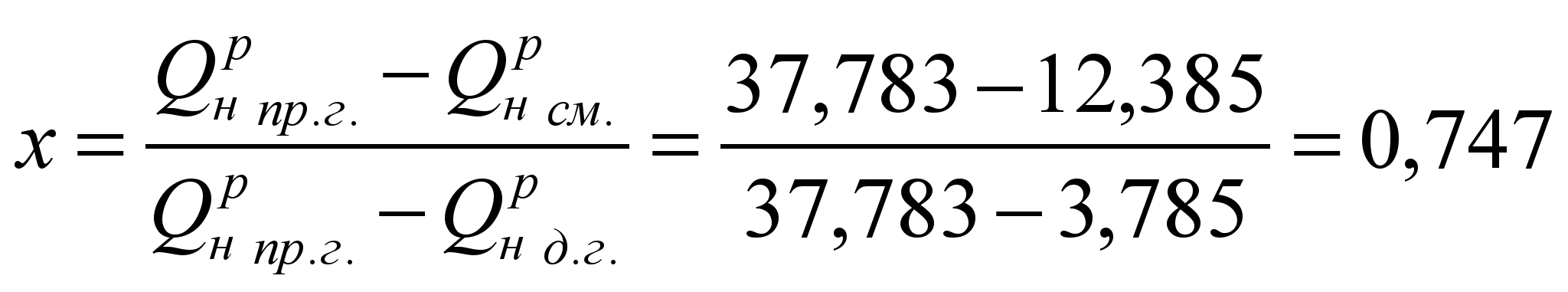 .
.
у = (1-х) = 1-0,747 = 0,253.
Состав смешанного газа, %.
;
Таблица 2. Состав природно-доменной смеси.
| CO | CO 2 | CH 4 | C 2 H 6 | C 3 H 8 | C 4 H 10 | N 2 | H 2 | H 2 O | ? |
| 20,48 | 9,1196 | 21,7877 | 1,0314 | 0,7448 | 0,4641 | 41,0975 | 1,0185 | 3,8769 | 100 |
Проверка:
Погрешность: 0,004%.
4. Плотность ПДС и воздуха.
Плотность ПДС.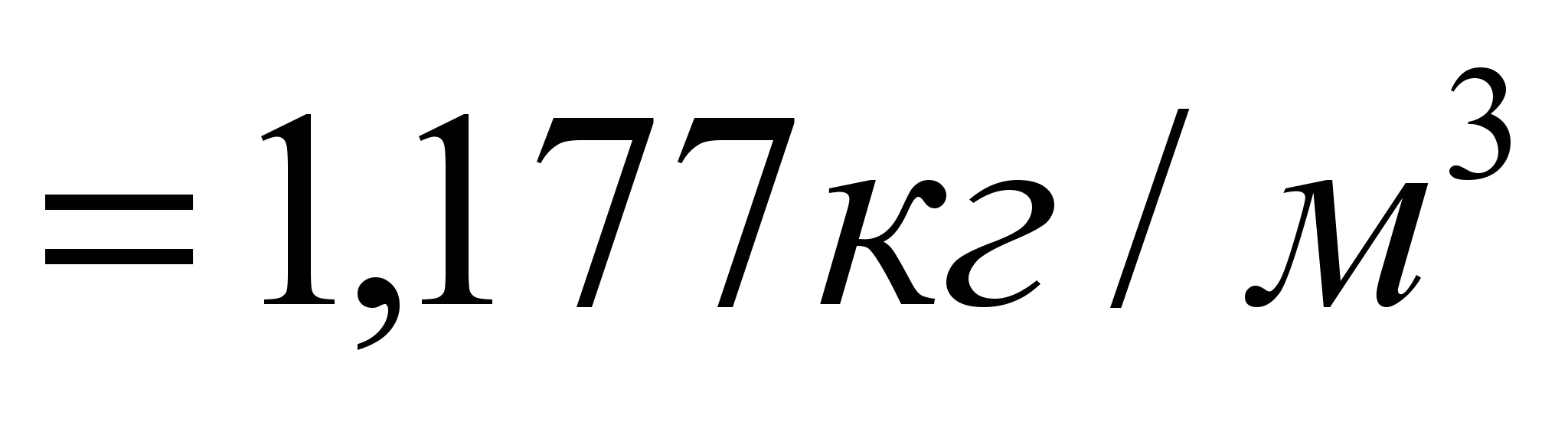 .
.
Плотность воздуха.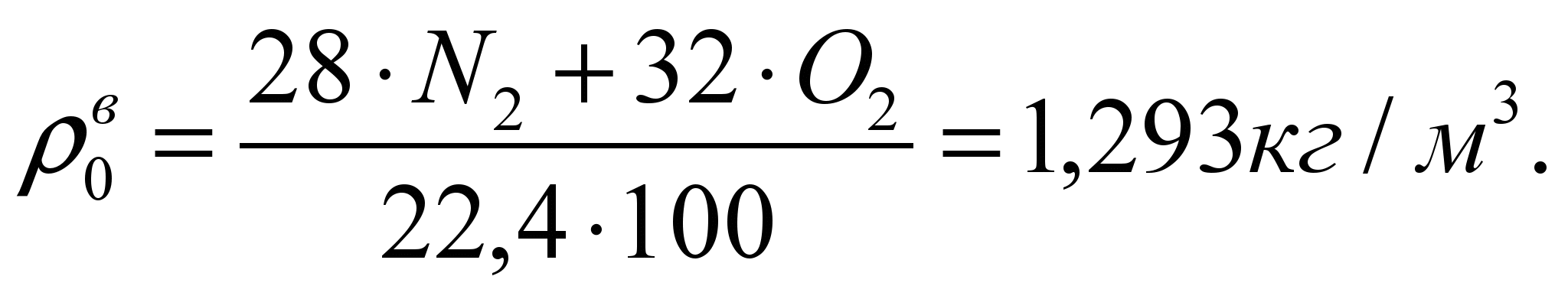
5. Расход воздуха, необходимого для сжигания единицы топлива.
Теоретический расход воздуха (n = 1).
Действительный расход воздуха (n = 1,14).
6. Расчет количества и состава продуктов сгорания.
Объем углекислого газа в ПГ:
Объем водяных паров в ПГ:
Объем азота в ПГ:
Объем избыточного кислорода в ПГ: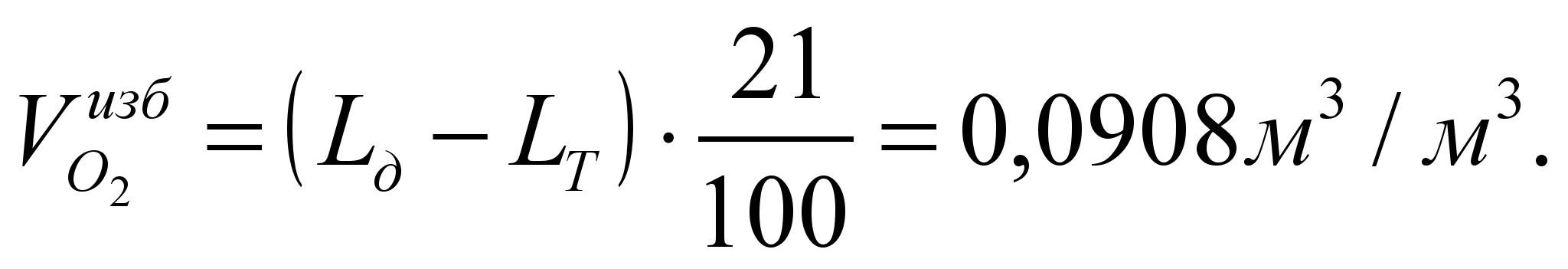
Общее количество ПС:
Состав ПС: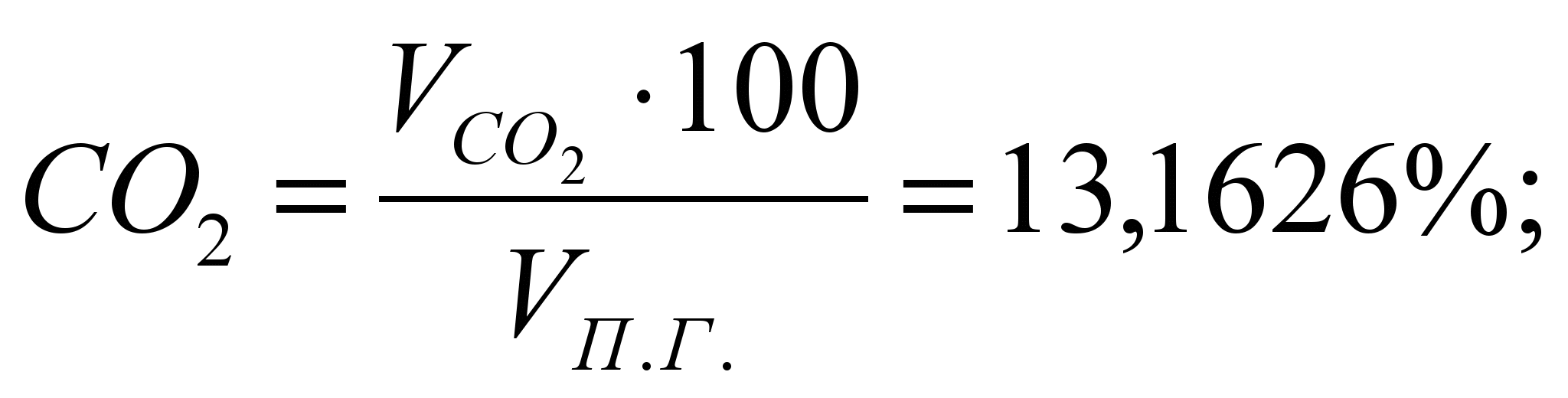
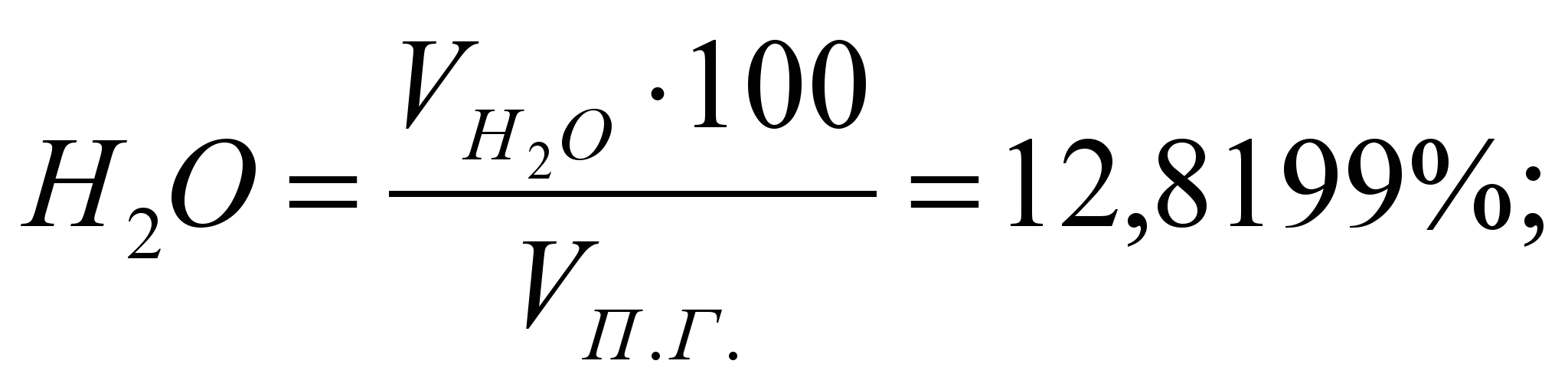
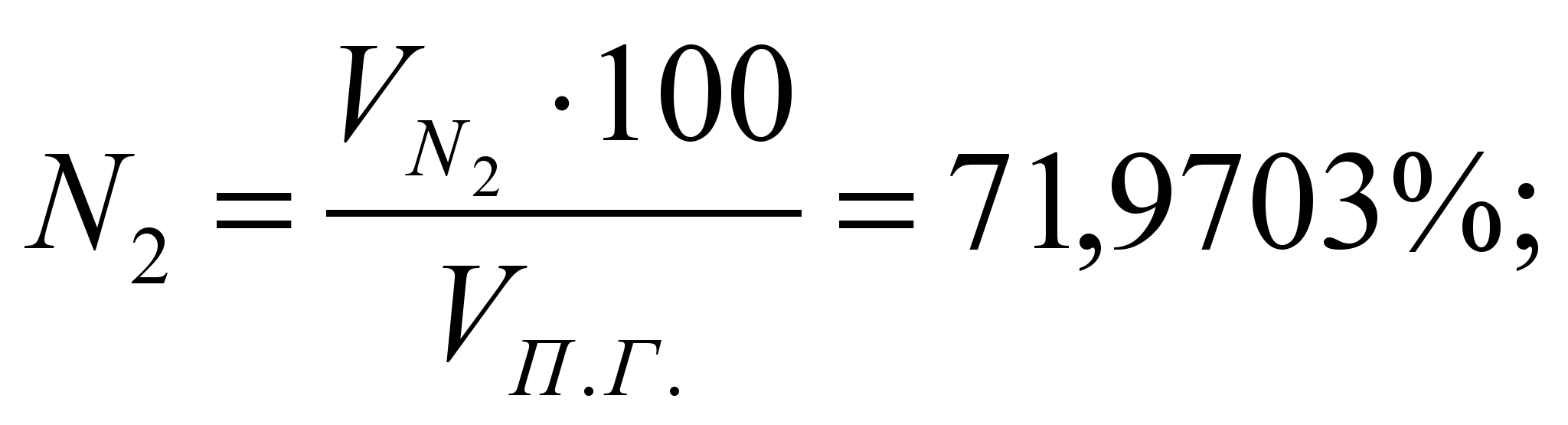
![]()
Таблица 3. Состав продуктов сгорания.
| Продукты сгорания | СО 2 | Н 2 О | N 2 | O 2 | ? |
| % | 13,1626 | 12,8199 | 71,9703 | 2,0472 | 100 |
Плотность ПС:
7. Материальный баланс процесса горения.
| Приход, кг | Расход, кг | Невязка баланса, % |
| 1. Газ:
| Продукты сгорания: | 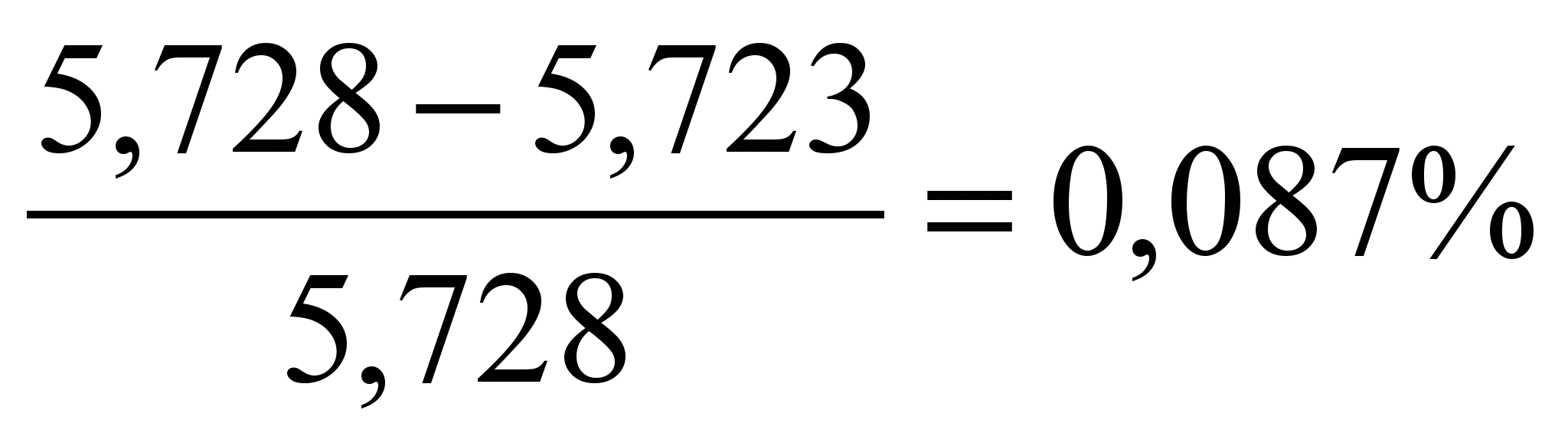 |
| 2. Воздух:
|
||
| Всего: 5,728кг | 5,723кг |
8. Определение калориметрической температуры горения.
Находим начальную энтальпию продуктов сгорания 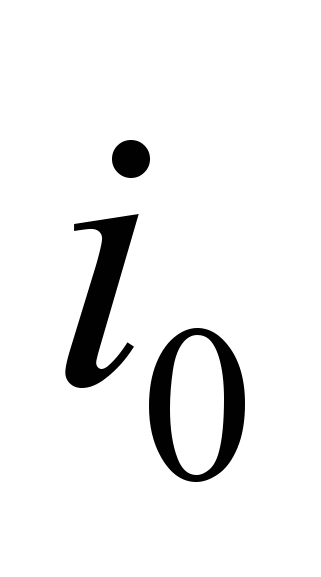 по формуле, где известно физическое тепло подогретого газа и воздуха.
по формуле, где известно физическое тепло подогретого газа и воздуха.
Физическое тепло газа:
где 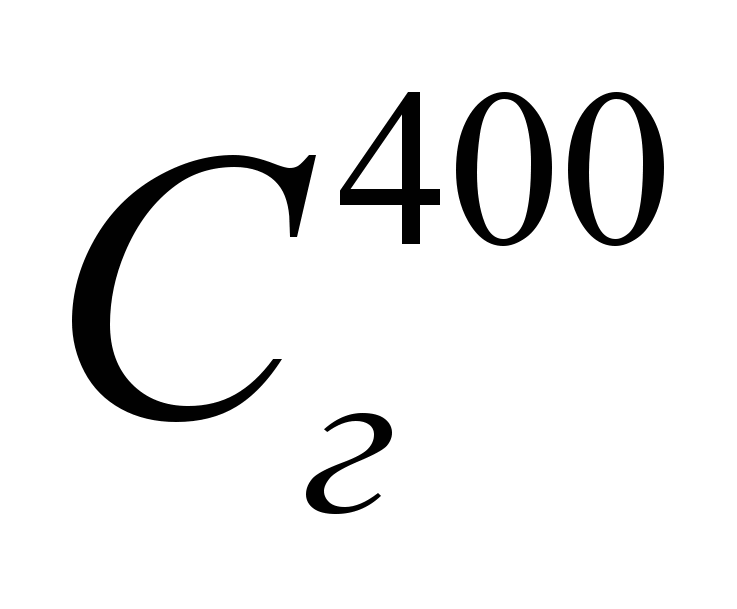 – теплоемкость подогретого газа при t = 400 o C, найденная по формуле:
– теплоемкость подогретого газа при t = 400 o C, найденная по формуле:
где: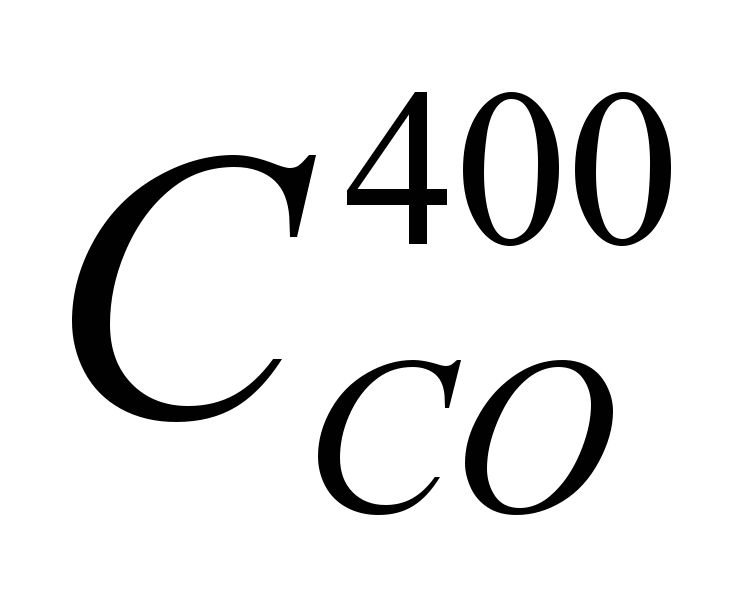
Физическое тепло подогретого воздуха:
.
Начальная энтальпия продуктов сгорания: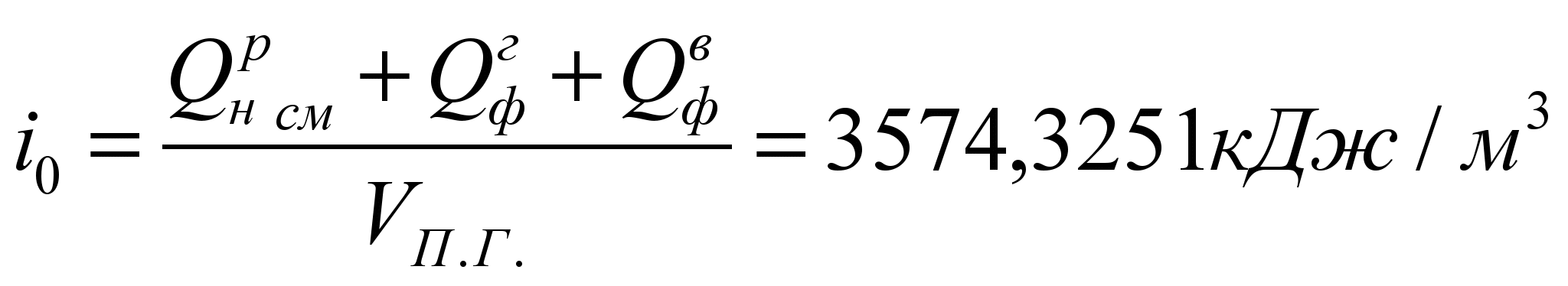 .
.
По величине , используя таблицу №7 (там же), находим приближенное значение 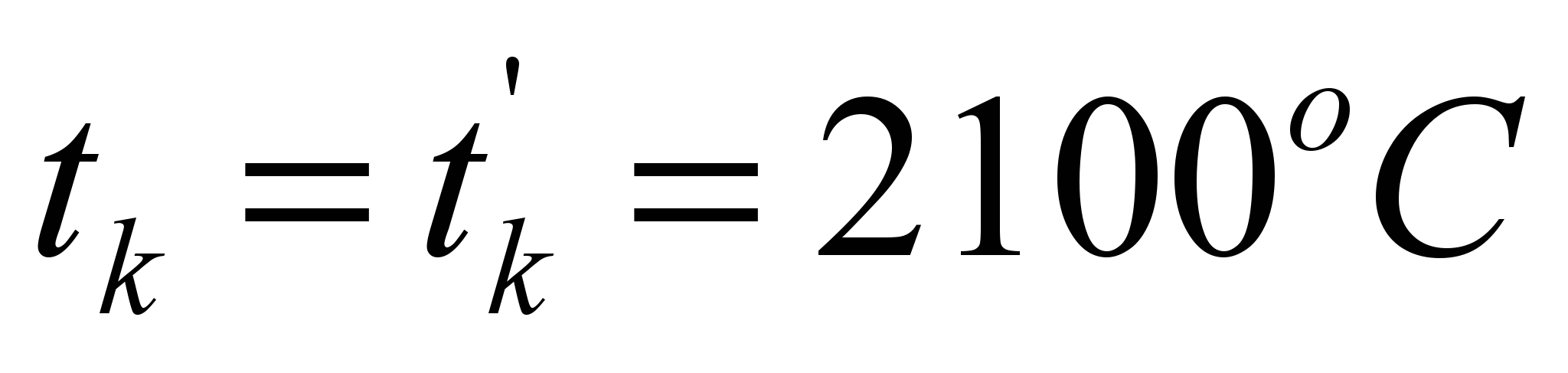 .
.
Определяем энтальпию продуктов горения при этой температуре:![]()
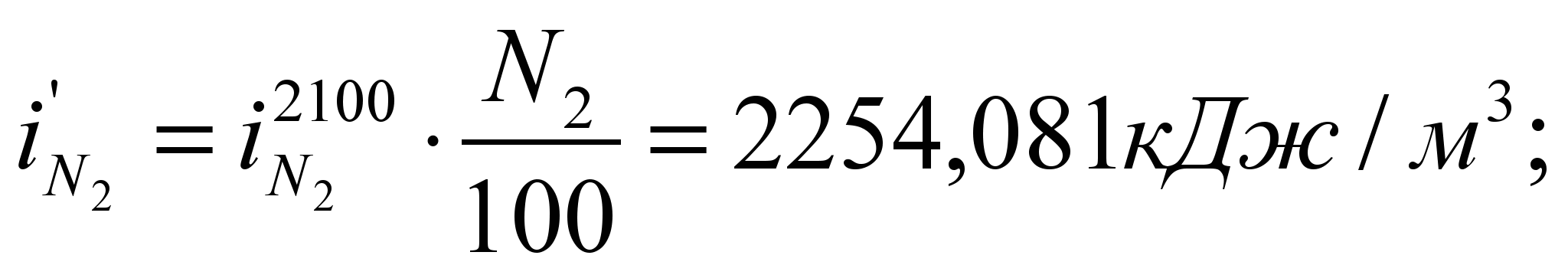
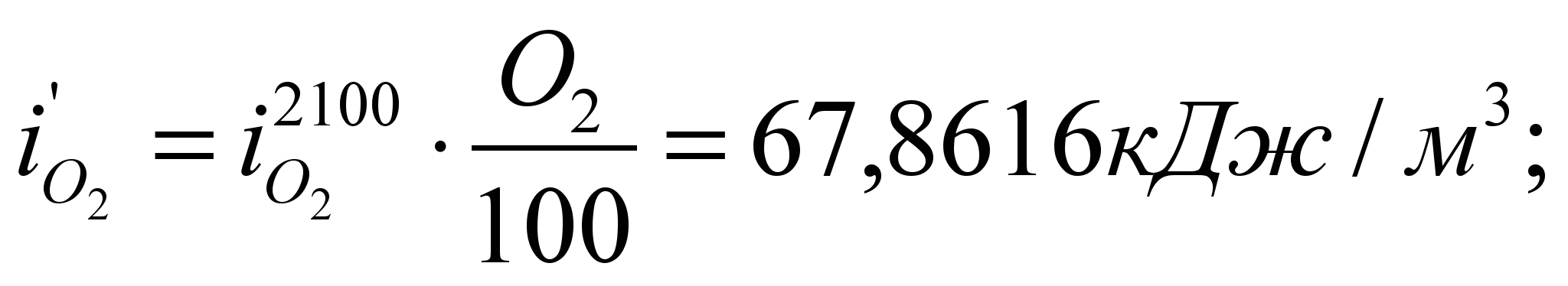
Значения 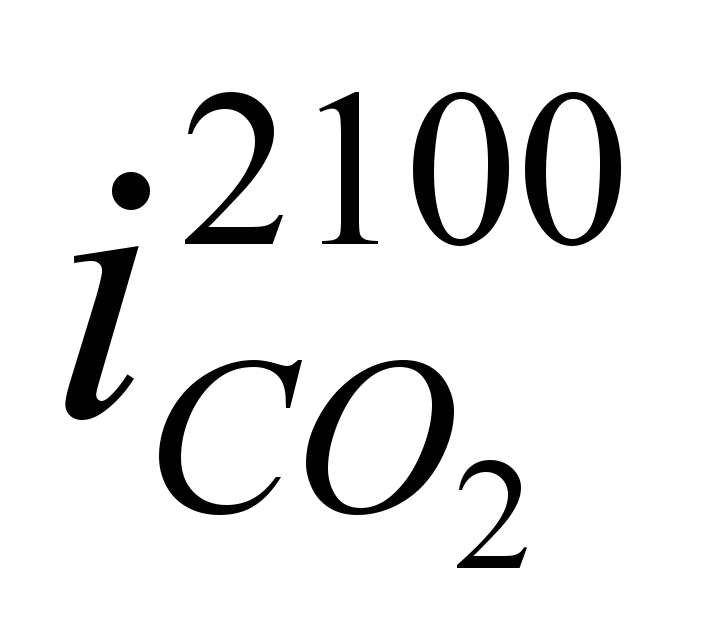 ,
, 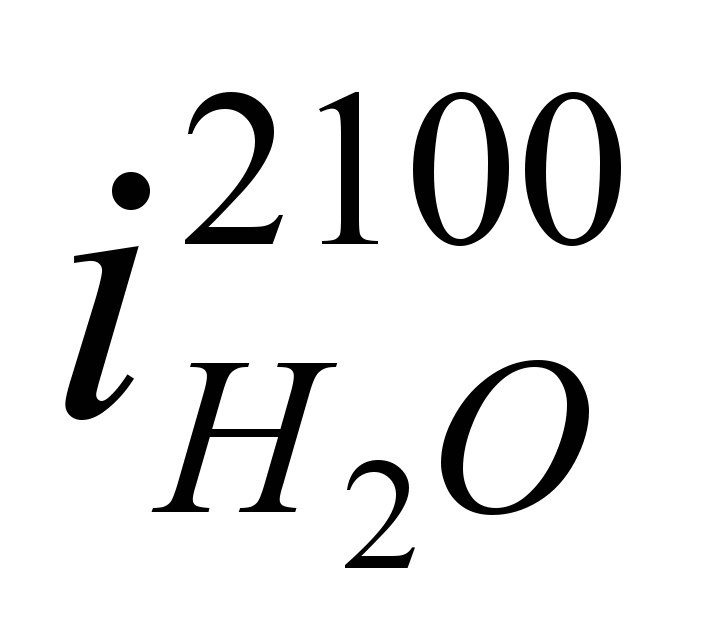 и т.д. находим из таблицы №6 (там же).
и т.д. находим из таблицы №6 (там же).
Полученное значение 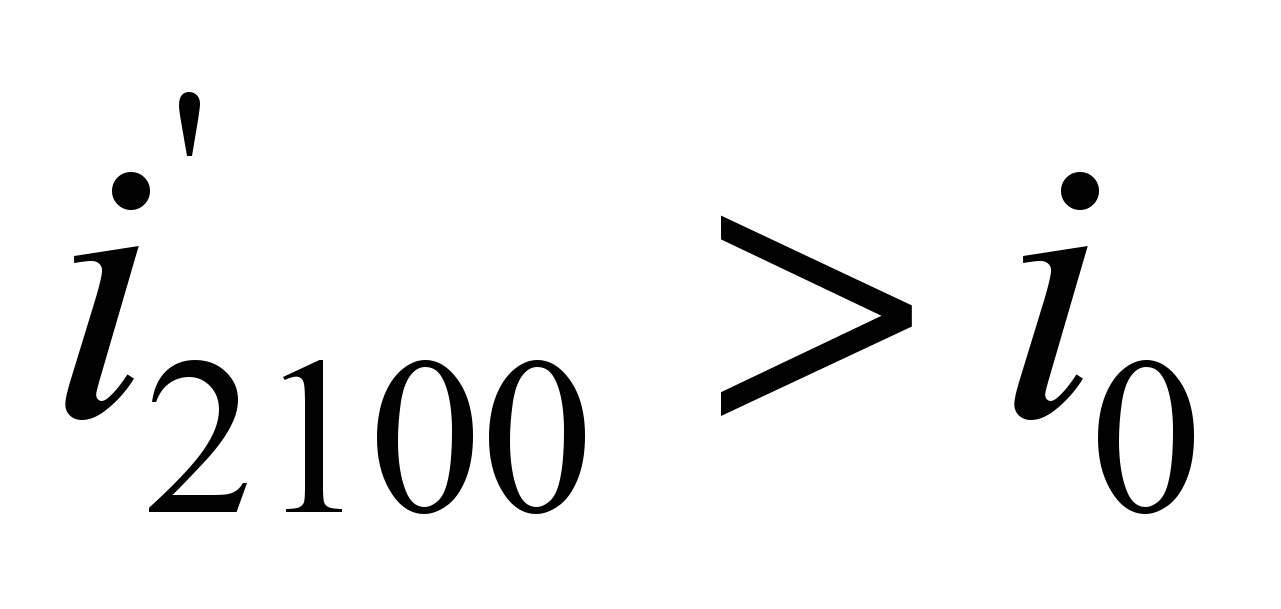 , значит,
, значит, ![]() .
.
Находим 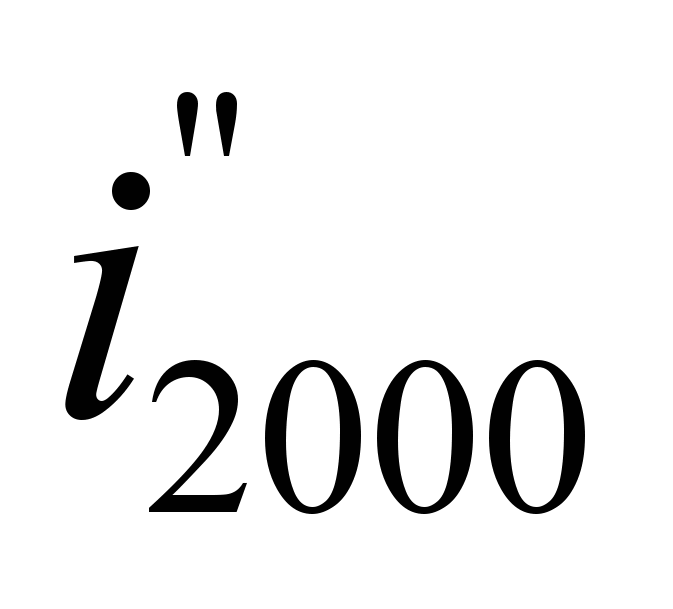 – энтальпию продуктов сгорания при 2000 о С:
– энтальпию продуктов сгорания при 2000 о С: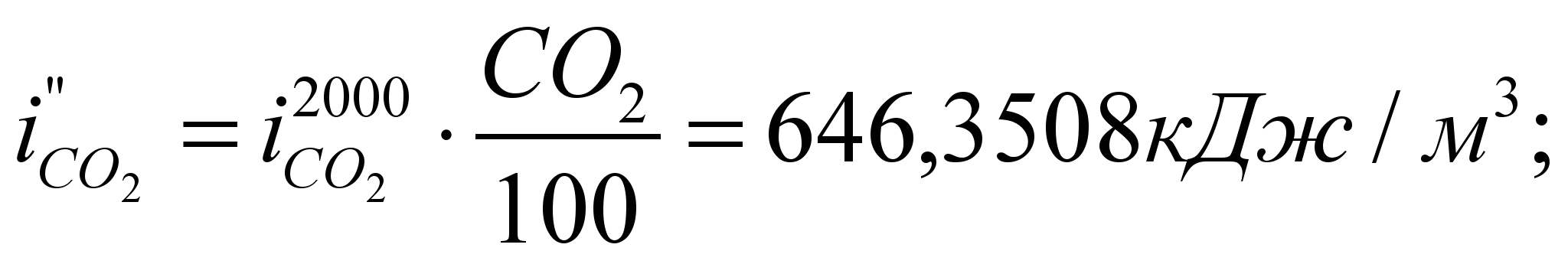
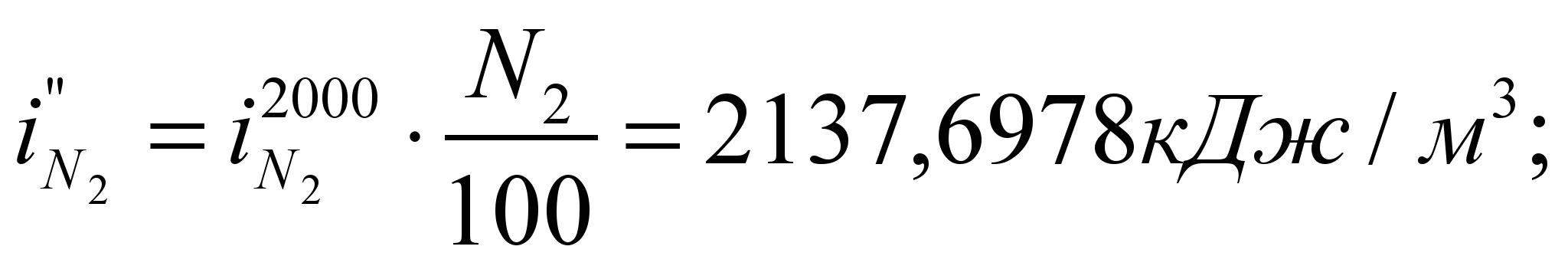
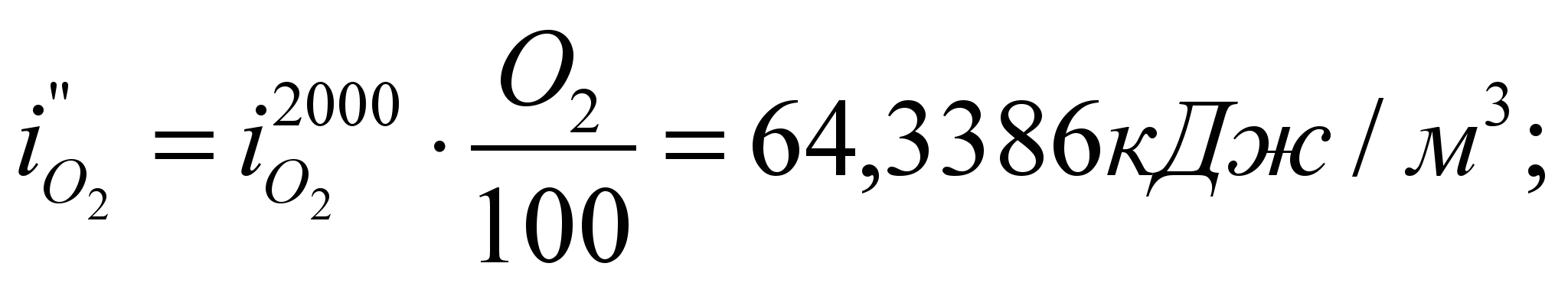
Получилось, что 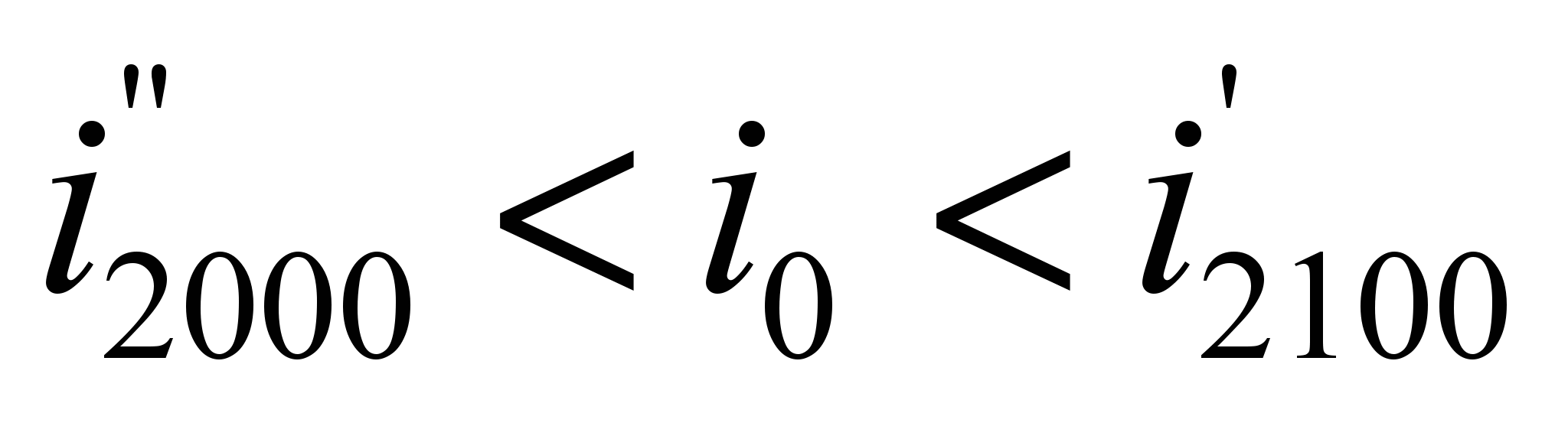 , т.е. действительно калориметрическая температура
, т.е. действительно калориметрическая температура 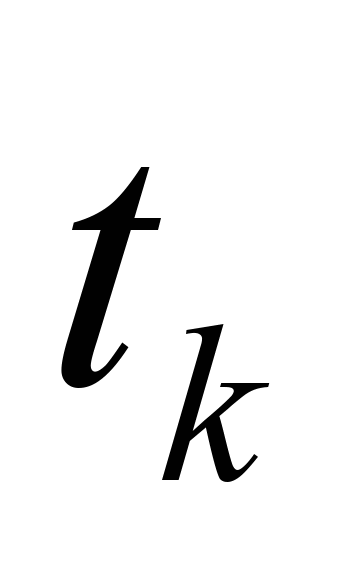 лежит в интервале
лежит в интервале 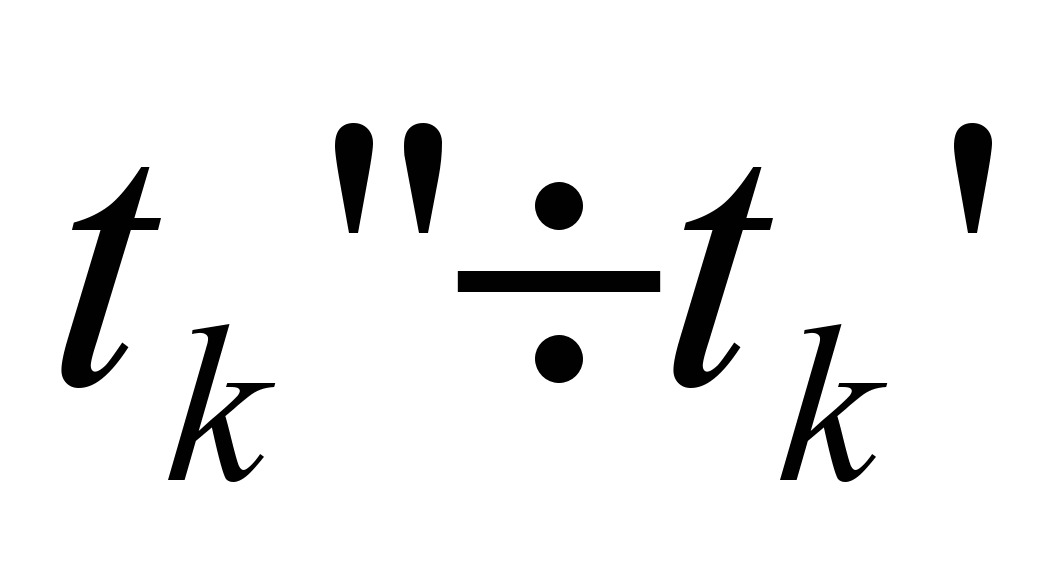 (
(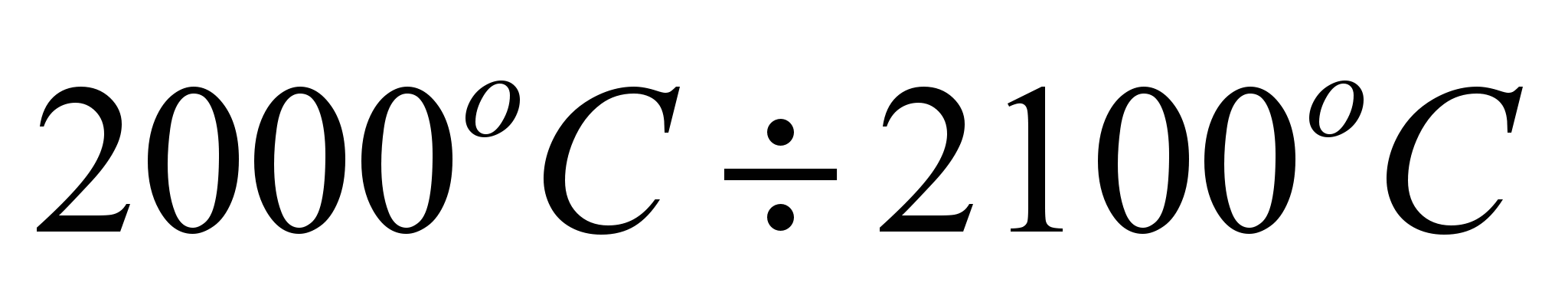 ), которая равна:
), которая равна: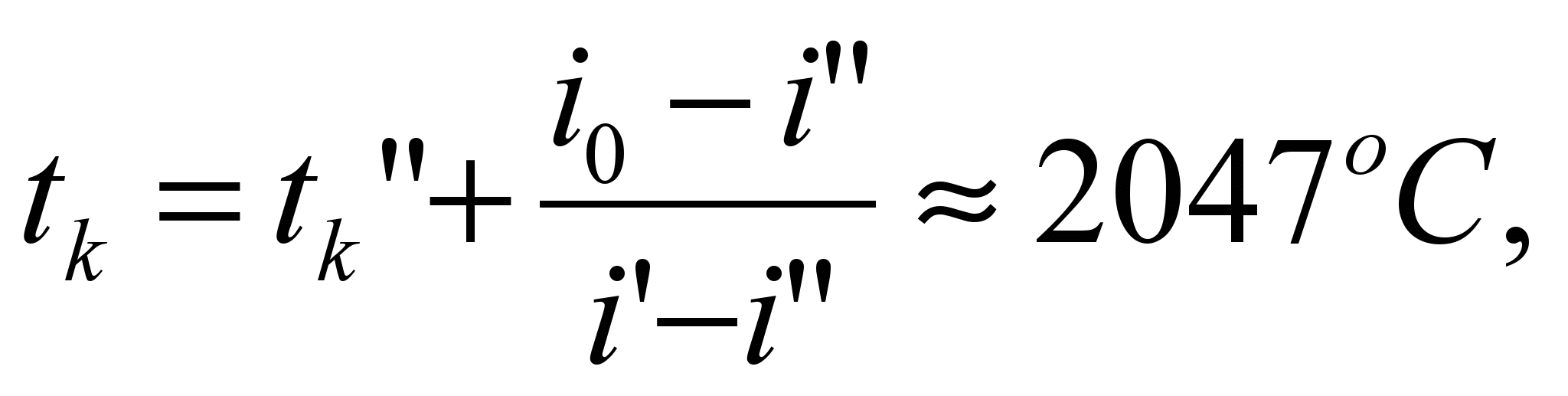 .
.
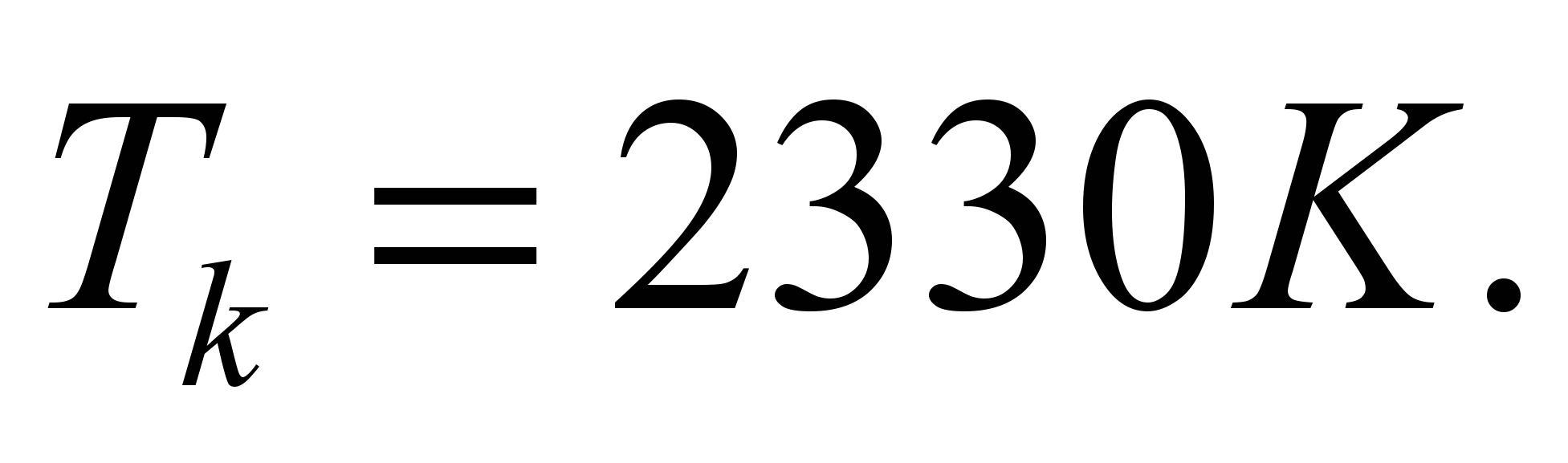
3.4.1 Горение газообразного топлива
Горение газов происходит в объеме и относится к гомогенному горению. Оно может происходить как в кинетической, так и в диффузионной области.
3.4.1.1 Кинетическое горение
После того, как произошло воспламенение, наступает процесс распространения пламени, связанный с постоянной передачей тепла от сгоревших к новым порциям топлива. Подобная передача тепла определяется законами теплопроводности и диффузии, и сильно зависит от характера пламени. Если пламя распространяется в неподвижной смеси или смеси, движущейся ламинарно, то основной формой передачи тепла будет молекулярная теплопроводность. Подобный чисто теплопроводный процесс получил название нормального горения.
При турбулентном движении газо – окислительной смеси большую роль приобретает турбулентная диффузия. При некоторых условиях распространение пламени происходит с огромной скоростью и имеет характер взрывной волны. Подобное распространение пламени получило название детонационного горения или просто детонации.
Важнейшими факторами, влияющими на скорость распространения нормального горения, являются состав горючей смеси, предварительная температура подогрева смеси или отдельных ее компонентов и давление.
Для всех горючих газов существует оптимальное соотношение газа и воздуха, при котором скорость нормального горения достигает максимальной величины. При этом максимум скорости нормального горения никогда не соответствует стехиометрическому соотношению, а всегда смещен в сторону избыточного содержания газа в горючей смеси. Температура горения (или тепловыделение) достигает своего наибольшего значения именно при стехиометрическом соотношении.
Горение при турбулентном режиме более распространенный случай в металлургической практике, чем горение в спокойной или ламинарно движущейся среде. На скорость турбулентного горения и на состояние фронта горения большое влияние оказывает общий уровень турбулентности потока и сам процесс горения, поскольку при определенных условиях возникает неустойчивость фронта горения.
3.4.1.2 Диффузионное горение
В настоящее время широко распространен диффузионный метод сжигания газообразного топлива, при котором смешение и горение происходят в одном объеме. И при кинетическом, и при диффузионном горении образуется фронт горения, в котором горючее и окислитель находятся в стехиометрическом соотношении. Достижение стехиометрического соотношения, которое при наличии постоянного поджигателя (в металлургических печах всегда есть поджигатель) обеспечивает необходимые условия для протекания процесса горения, зависит от характера перемешивания топлива с воздухом. Поэтому процессы смешения при диффузионном горении играют первостепенную роль.
Диффузионные пламена имеют сложный турбулентный характер и изучены пока недостаточно.
3.4.2 Горение жидкого топлива
В условиях промышленных печей жидкое топливо сжигают в распыленном состоянии.
Процесс горения жидкого топлива складывается из следующих стадий:
Распыливание,
Воспламенение, которому предшествует и способствует процесс смешения, подогрева и испарения,
Горение капли жидкого топлива.
Процесс распыливания топлива основан на дроблении жидкости распылителем. Дробление будет происходит в том случае, если давление движущегося распылителя будет превышать действие поверхностного натяжения.
Воспламенение жидкого топливапроисходит так: жидкое топливо, попав в среду с высокой температурой, начинает испаряться. Около поверхности капли образуется паро – воздушная смесь, которая воспламеняется первой. Температура, при которой происходит воспламенение паро – воздушной смеси, называется температурой вспышки топлива. Обычно температура кипения жидкого топлива ниже температуры воспламенения.
Горение капли. Все процессы, из которых складывается горение топлива, совершаются или на поверхности, или около поверхности капли.
Температура кипения жидких топлив всегда ниже температуры воспламенения, поэтому горение жидкого в основном происходит в паровой фазе. Процессы горения паро – воздушной смеси и испарения тесно связаны между собой. При горении жидкого топлива осуществляется теплообмен между газовой средой и поверхностью жидкости, т. е. между средами, находящимися в разных агрегатных состояниях, что придает всему процессу гетерогенный характер
Общее время горения капли находят из анализа изменения размеров капли в связи с процессами тепло – и массопереноса. Оно прямо пропорционально плотности, размеру капли и скрытой теплоте капли и обратно пропорционально теплопроводности капли, а также перепаду температур между газовой средой и поверхностью капли.
3.4.3 Горение твердого топлива
Горение твердого топлива относится к гетерогенному.
Процесс горения твердого топлива складывается из следующих стадий:
Подогрев и подсушка топлива,
Процесс пирогенного разложения топлива с выделением летучих и образованием коксового остатка,
Горение летучих,
Горение коксового остатка.
Процесс выделения летучих, т. е. горючей смеси различных газообразных составляющих – Н 2 , СО, СН 4 , С m H n и др., протекает при подогреве топлива до 200 ˚С и выше. Температура начала выделения летучих зависит от возраста угля. Чем "старше" уголь, чем выше в нем содержание углерода, тем при более высокой температуре начинается процесс выделения летучих. Летучие в процессе горения твердого топлива играют важную роль, которая различна при горении кускового топлива и угольной пыли.
При горении кускового топлива летучие выделяются при сравнительно умеренных температурах, смешиваются с воздухом и воспламеняются первыми. Таким образом, горением летучих начинается процесс горения всего топлива. Тепло, выделяемое при горении летучих, способствует повышению температуры и дальнейшему развитию процесса горения. Горение углерода начинается уже после завершения выхода летучих. Процесс горения самого углерода продолжителен и он определяет время протекания всего процесса.
При сжигании угольной пыли в связи с огромной суммарной поверхностью угольных частиц основная масса летучих не успевает выделиться до момента воспламенения частиц, поэтому летучие сгорают вместе с углеродом.
3.4.4 Расчеты горения топлива
При сжигании топлива в промышленных печах в качестве окислителя используют кислород, содержащийся в воздухе или в обогащенном кислородом дутье. В результате горения образуются продукты сгорания и развивается определенная температура.
3.4.4.1 Определение расхода воздуха
Расход воздуха можно определять в объемных единицах и в единицах массы. В объемных единицах рассчитывают газообразное топливо, в единицах массы – жидкое и твердое топливо.
В качестве примера рассмотрим горение топлива, состоящего из 98 % СН 4 и
СН 4 + 2 О 2 = СО 2 + 2 Н 2 О,
из которой следует, что для сжигания 1 кмоль СН 4 требуется 2 кмоль О 2 . Но объем 1 кмоль любого газа одинаков для всех газов и при нормальных условиях равен 22,4 м 3 , следовательно для сжигания 1 м 3 СН 4 требуется 2 м 3 О 2 . В рассматриваемом примере в 1 м 3 газа содержится 0,98 м 3 СН 4 , для сжигания которого потребуется 0,98 ∙ 2 = 1,96 м 3 О 2 . В сухом воздухе доля кислорода по объему составляет 21 %, а остальные 79 % приходится практически полностью на азот. Значит, количество азота в воздухе в 79/21=3,76 раза больше количества кислорода. Поэтому расход воздуха для сжигания 1 м 3 газа указанного состава будет равен 1,96 + 1,96 ∙ 3,76=1,96 + 7,38 = 9,34 м 3 .
При горении топлива полученные на основе химических реакций количества кислорода и воздуха представляют те наименьшие количества, которые необходимы для полного окисления единицы горючего вещества. Такое наименьшее необходимое количество воздуха называют теоретическим. на прктике для более полного сжигания требуется подавать количество воздуха, несколько превышающее теоретическое. Величина показывающая отношение действительного расхода воздуха к теоретическому расходу называют коэффициентом расхода воздуха.
Изменение величины коэффициента расхода воздуха влечет за собой изменение количества воздуха, подаваемого для горения. Так, для рассмотренного выше примера горения газа при n=1,2 потребуется
1,96 ∙ 1,2 = 2,35 м 3 О 2 и 2,35 + 2,35 ∙ 3,76 = 11,19 м 3 воздуха.
3.4.4.2Определение количества и состава продуктов сгорания
Рассмотрим пример горения газа (98 % СН 4 и 2 % N 2) сначала при коэффициенте расхода воздуха, равным 1. Определим последовательно количества каждой составляющей продуктов сгорания. При сжигании 1 м 3 СН 4 образуется 1 м 3 СО 2 и 2 м 3 Н 2 О, а при сжигании 0,98 м 3 СН 4 образуется 0,98 м 3 СО 2 и 1,96 м 3 Н 2 О.
Кроме того, вносится азота:
с воздухом. . . . . 1,96 ∙ 3,76 = 7,38
с газом. . . . . . . . . . . . . . . . . . . 0,02
––––––––––––––––––––––
Итого. . . . . 7,40
Полное количество продуктов сгорания составит 0,98 + 1,96 + 7,40 = 10,34 м 3 .
СО 2 . . . . . . . . 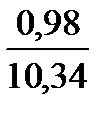 ∙ 100 = 9,45
∙ 100 = 9,45
Н 2 О. . . . . . . . 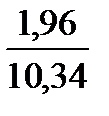 ∙ 100 = 18,9
∙ 100 = 18,9
N 2 . . . . . . . . . 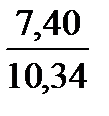 ∙ 100 = 71,65
∙ 100 = 71,65
При сжигании газа с коэффициентом расхода воздуха, большем единицы, количество и состав продуктов сгорания изменяются. Например, при n = 1,2 в продуктах сгорания рассматриваемого состава будет 0,98 м 3 СО 2 ; 1,96 м 3 Н 2 О; 1,96 ∙ 1,2 – 1,96 = 0,39 м 3 О 2 и 1,96 ∙ 1,2 ∙ 3,76 + 0,02 = 8,86 м 3 N 2 .
Полное количество продуктов сгорания составит 0,98 + 1,96 + 0,39 + 8,86 = 12,19 м 3 .
Состав продуктов сгорания будет следующий, %:
СО 2 . . . . . . . . 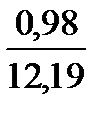 ∙ 100 = 8,05
∙ 100 = 8,05
Н 2 О. . . . . . . . 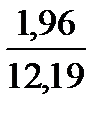 ∙ 100 = 16,1
∙ 100 = 16,1
О 2 . . . . . . . . . . 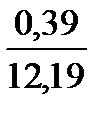 ∙ 100 = 3,2
∙ 100 = 3,2
N 2 . . . . . . . . . 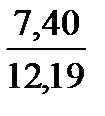 ∙ 100 = 72,65
∙ 100 = 72,65
–––––––––––––––––––––––––––––––
Итого. . . . . . . . . . . . . 100
При расчетах горения необходимо составлять материальный баланс, определяя массы исходных веществ и образующихся продуктов сгорания. Для рассмотренного выше примера горения в воздухе газа (98 % СН 4 и 2 % N 2) при n = 1 материальный баланс будет выглядеть следующим образом:
Поступило, кг: Получено, кг:
СН 4 . . . . .0,98 ∙ 16 / 22,4 = 0,7 СО 2 . . . . . . 0,98 ∙ 44 / 22,4 = 1,925
О 2 . . . .. . .1,96 ∙ 32 / 22,4 = 2,8 Н 2 О. . . . . .1,96 ∙ 18 / 22,4 = 1,575
N 2 . . (7,38 + 0,02) ∙ 28 / 22,4 = 9,25 N 2 . . . . . . . . 7,4 ∙ 28 / 22,4 = 9,25
–––––––––––––––––––––––––––––– ––––––––––––––––––––––––––––––
Итого. . . . . . . . . . 12,75 Итого. . . . . . . . . . . . 12,75
При составлении материального баланса погрешность не должна превышать 5 %.
3.4.4.3Определение температуры горения
Под температурой горения понимают ту температуру,которую приобретают продукты сгорания в результате сообщения им тепла, выделенного при сжигании. Различают теоретическую и калориметрическую температуры горения.
Теоретическую температуру горения t т определяют с учетом процессов диссоциации, протекающих при образовании продуктов сгорания:
где - теплота сгорания топлива, кДж/м 3 или кДж/кг;
q дисс – тепло, израсходованноеина процессы диссоциации, кДж/м 3 или кДж/кг;
V пр – объем продуктов сгорания, образующихся при сгорании единицы топлива,
с – объемная теплоемкость продуктов сгорания, кДж/(м 3 ∙ град) или
кДж/(кг ∙ град).
Калориметрическую температуру t к определяют из условия полного сгорания топлива и использования всего выделившегося при горении тепла только на повышение температуры продуктов сгорания при адиабатных условиях (отсутствие теплообмена с внешней средой) и n = 1.
При подогретом воздухе (или топливе) калориметрическую температуру определяют по выражению:
где Q ф – физическое тепло подогретых воздуха и топлива.
Газообразные продукты сгорания любого топлива представляют собой смесь различных газообразных составляющих. Каждой из этих составляющих при той или иной температуре присуща определенная величина теплоемкости. Это дает возможность определить теплоемкость теплоемкость продуктов сгорания в целом для соответствующей температуры. Например, теплоемкость продуктов сгорания, состоящих из 9,45 % СО 2 , 18,9 % Н 2 О и 71,65 % N 2 при температуре 1500 ˚ С может быть определена следующим образом.
Объемные теплоемкости при этой температуре составят:
для СО 2 2,3636 кДж/(м 3 ∙ град),
для Н 2 О 1,8389 кДж/(м 3 ∙ град),
для N 2 1.447 кДж/(м 3 ∙ град).
В 1 м 3 продуктов сгорания содержится 0,0945 м 3 СО 2, 0,189 м 3 Н 2 О, 0,7165 м 3 N 2 .
Следовательно, теплоемкость 1 м 3 продуктов сгорания будет равна:
СО 2 . . . . . .2,3636 ∙ 0,0945 = 0,223
Н 2 О. . . . . . 1,8389 ∙ 0,189 = 0,348
N 2 . . . . . . . .1,447 ∙ 0,7165 = 1,035
–––––––––––––––––––––––––––––
Итого. . . . . .. . . . . . 1,606
Кроме теплоемкостей пользуются также величинами энтальпий. Энтальпия представляет собой произведение теплоемкости газа при постоянном давлении на температуру:
i = с р t кДж/м 3 .
Например, энтальпия СО 2 при температуре 1500 ˚ С равна:
i (СО 2) = 2,3636 ∙ 1500 = 3545,34 кДж/м 3 .
3.4.4.4Основные формулы для расчета горения топлива
Сведем все формулы, необходимые для расчета горения топлива, в единую таблицу.
Таблица 3.2 – Основные формулы для расчета горения топлива
| Искомый параметр | Жидкое и твердое топливо | Газообразное топливо |
| Пересчет на рабочий состав | | |
| Состав смеси |
где |
|
| Низшая теплота сгорания | ||
| Таблица 3.2 Продолжение | ||
| Расход кислорода на горение при n=1 | V(О 2)=0,01(1,867С Р +5,6Н Р + +0,7(S Р -О Р)) | V(О 2)=0,01(0,5(СО+Н 2 +3Н 2 S)+∑(n+m/4)С n Н m) |
| Расход сухого воздуха | V В =n(1+k)V(О 2), где k=79/21=3,76;n – коэффициент расхода воздуха | |
| Объемы компонентов продуктов сгорания | V(RО 2)=0,01(1,867С Р +0,7S Р) RО 2 =СО 2 +SО 2 V(Н 2 О)=0,01(11,2Н Р + +1,242W Р) V(N 2)=0,008N Р +nkV(О 2) V(О 2)"=(n-1)V(О 2) | V(RО 2)=0,01(СО 2 +SО 2 +СО+ +Н 2 S+∑nС n Н m) V(Н 2 О)=0,01(Н 2 О+Н 2 + Н 2 S+ +0,5∑mС n Н m) V(N 2)=0,01N 2 +nkV(О 2) V(О 2)"=(n-1)V(О 2) |
| Объем продуктов сгорания | V ПС = V(RО 2)+ V(Н 2 О)+ V(N 2)+ V(О 2)" | |
| Калориметрическая температура горения | |
|
| Энтальпия продуктов сгорания | Истинная
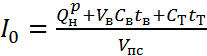 При температуре t К "
При температуре t К "
|
|
| Действительная температура продуктов сгорания | t Д =η пир t К, где η пир - пирометрический коэффициент для топочных камер η пир =0,95 для мартеновских печей η пир =0,85 – 0,9 для садочных печей η пир =0,8 – 0,85 для проходных и протяжных печей η пир =0,7 – 0,75 |
30. /4 курс/Теоретические основы теплотехники/Конспект лекций/ОТТ. Тема 8c. Кратко.doc
31. /4 курс/Теоретические основы теплотехники/Конспект лекций/ОТТ. Тема 9с. Кратко.doc
32. /4 курс/Теоретические основы теплотехники/Метод. ТОТзаочн.doc
33. /4 курс/Теоретические основы теплотехники/Раб. пр. ТОТ.doc Національна металургійна академія україни
Методичні вказівки та індивідуальні завдання до вивчення дисципліни "Теоретичні основи теплотехніки" для студентів спеціальностей 090202, 090218
9. Теплопроводность
8. Теоретические основы теплотехники 1998г
7. Тепловые двигатели
Закон термодинамики
6. Теоретические основы теплотехники 1998г
Тема термодинамические процессы
Закон термодинамики
Тема теплоёмкость газов
Тема основные термодинамические понятия и законы
Тема 15. Твердое и жидкое топливо и их сжигание >15 Расчет горения твердого и жидкого топлива Для расчета процессов горения твердого и жидкого топлива составляют материальный баланс процесса горения
Тема 14. Газообразное топливо и его сжигание
Топливо и его характеристики 13 Виды топлива и их особенности
12. Сложный теплообмен
11. Теплообмен излучением
10. Конвективный теплообмен
Національна металургійна академія України
Програма навчальної дисципліни Основи наукових дослiджень та технiка експерименту
Методичні вказівки до його виконання. Призначена для студентів напряму 050503 машинобудування
Методичні вказівки до виконання контрольної роботи з дисципліни "Основи математичного моделювання" для студентів спеціальності 090202
Методичні вказівки та контрольні завдання для студентів заочної
Методичні вказівки до вивчення дисципліни "Металообробні верстати", наведені: рекомендована література, робоча програма і пояснення до тем лекцій, лабораторних занять, питання з самоконтролю
Методичні вказівки до виконання контрольної роботи з дисципліни "Математичні моделі в розрахунках на еом"" для студентів напряму 050503
Методичні вказівки до виконання індивідуальних робіт з дисципліни «Мікроекономіка» Тематика індивідуальних завдань з дисципліни «Мікроекономіка»
Методичні вказівки до вивчення дисципліни «Електротехніка, електроніка і мікропроцесорна техніка», література, пояснення до виконання індивідуальних завдань
Методичні вказівки до вивчення матеріалу кожної теми та наводяться запитання для контролю якості засвоєння тем. Даються методичні вказівки до виконання контрольної роботи, а також варіанти вихідних даних для неї
Методичні вказівки і індивідуальні завдання з дисципліни «Історія інженерної діяльності» для студентів спеціальностей 090202, 090218, 092301
Методичні вказівки до самостійного вивчення тем, передбачених програмою дисципліни «Mенеджмент», завдання до контрольної роботи та методичні вказівки до її виконання
Тема 15. Теоретические основы теплотехники 1998г.
Тема 15. Твердое и жидкое топливо и их сжигание
15.1. Расчет горения твердого и жидкого топлива
Для расчета процессов горения твердого и жидкого топлива составляют материальный баланс процесса горения.
Материальный баланс процесса горения выражает количественные соотношения между исходными веществами (топливо, воздух) и конечными продуктами (дымовые газы, зола, шлак), а тепловой баланс - равенство между приходом и расходом теплоты. Для твердого и жидкого топлива материальный и тепловой балансы составляют на 1 кг топлива, для газообразной - на 1 м 3 сухого газа при нормальных условиях (0,1013 МПа, О °С). Объемы воздуха и газообразных продуктов также выражают в метрах кубических, приведенных к нормальным условиям.
При сжигании твердого и жидкого топлива горючие вещества могут окисляться с образованием оксидов различной степени окисления. Стехиометрические уравнения реакций горения углерода, водорода и серы можно записать так:
А) С+О 2 =СО 2 ;
Б) С+(1/2)О 2 =СО;
В) S+О 2 =SО 2 ; (15-1)
Г) H 2 +(1/2)О 2 =H 2 О;
При расчете объемов воздуха и продуктов сгорания условно принимают, что все горючие вещества окисляются полностью с образованием только оксидов с наивысшей степенью окисления (реакции а, в, г ).
Из уравнения (а) следует, что для полного окисления 1 кмоль углерода (12 кг) расходуется 1 кмоль, т. е. 22,4 м 3 , кислорода и образуется 1 кмоль (22,4 м 3) оксида углерода. Соответственно для 1 кг углерода потребуется 22,4/12 = 1,866 м 3 кислорода и образуется 1,866 м 3 СО 2 . В 1 кг топлива содержится С р /100 кг углерода. Для его горения необходимо 1,866С р /100 м 3 кислорода и при сгорании образуется 1,866 С р /100 м 3 CO 2 .
Аналогично из уравнений (в)
и (г) на окисление горючей серы ( s = 32), содержащейся в 1 кг топлива, потребуется (22,4/32) S р л /100 м 3 кислорода и образуется такой же объем SO 2 . А на окисление водорода (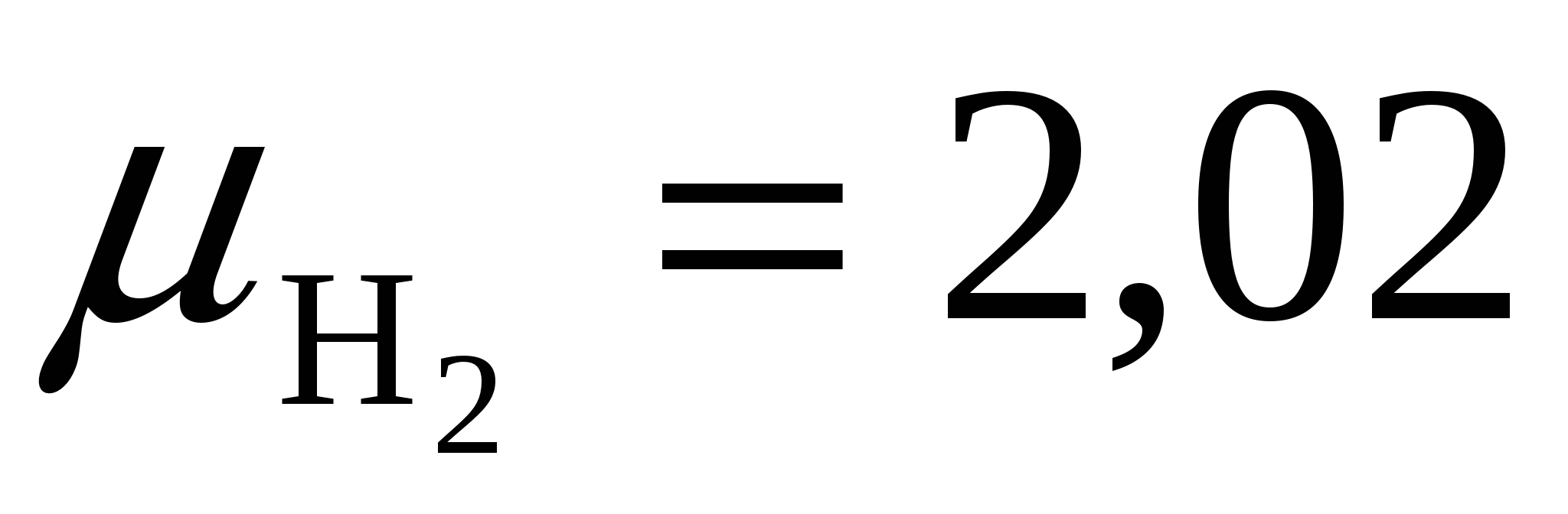 ), содержащегося в 1 кг топлива, потребуется 0,5(22,4/2,02) Н р /100 м 3 кислорода и образуется (22,4/2,02) Н р /100 м 3 водяного пара.
), содержащегося в 1 кг топлива, потребуется 0,5(22,4/2,02) Н р /100 м 3 кислорода и образуется (22,4/2,02) Н р /100 м 3 водяного пара.
Суммируя полученные выражения и учитывая кислород, находящийся в топливе (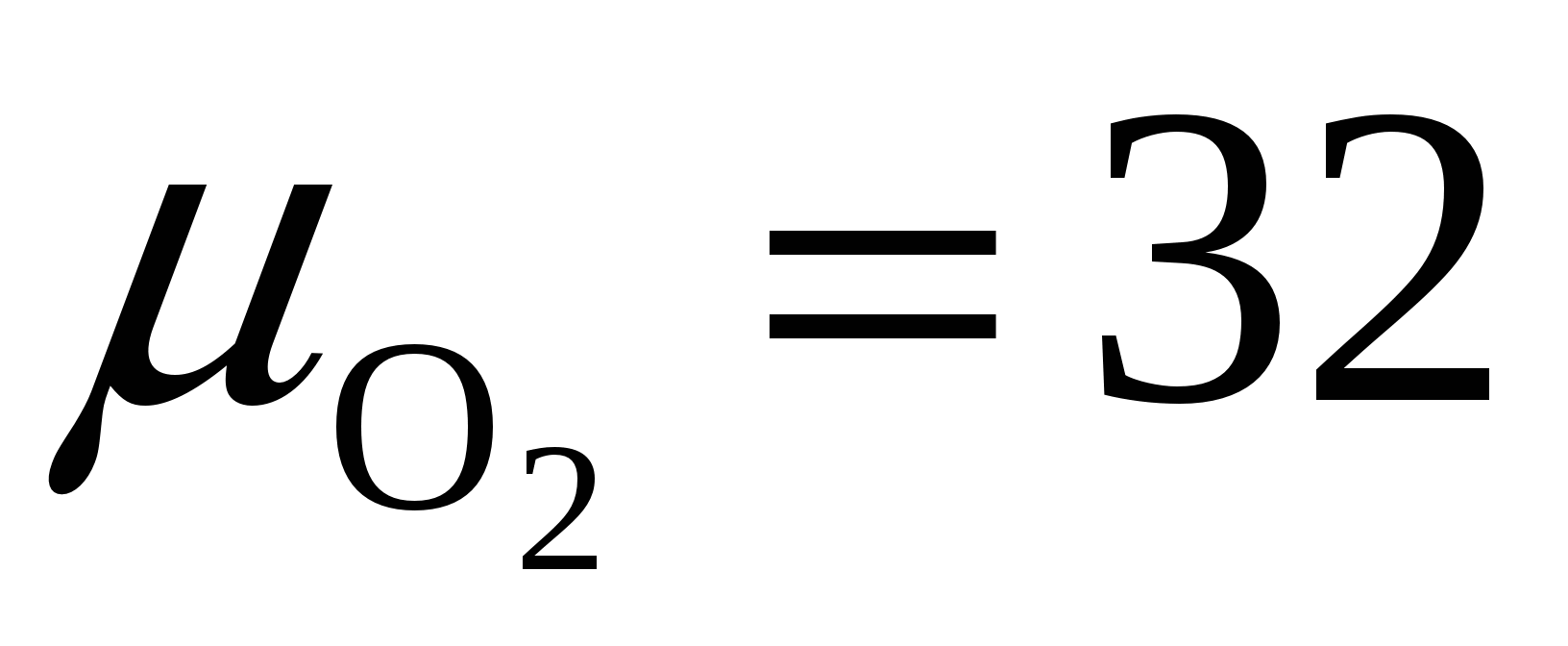 ), после несложных преобразований получим формулу для определения количества кислорода, теоретически необходимого для полного сжигания 1 кг твердого или жидкого топлива, м 3 /кг:
), после несложных преобразований получим формулу для определения количества кислорода, теоретически необходимого для полного сжигания 1 кг твердого или жидкого топлива, м 3 /кг:
В воздухе содержится кислорода примерно 21 % по объему, поэтому количество воздуха, теоретически необходимое для полного сжигания 1 кг топлива V 0 , м 3 /кг, составляет:
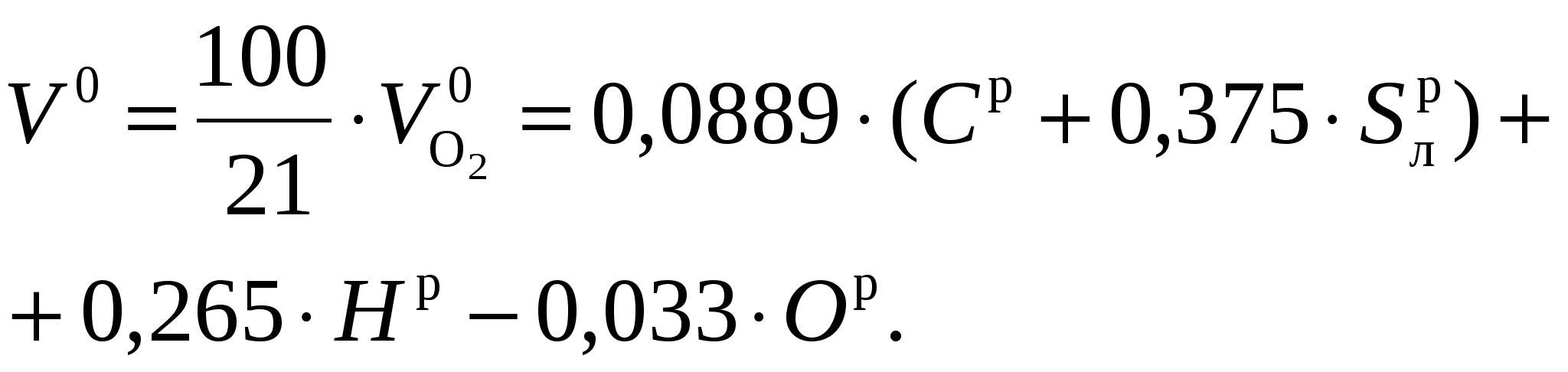 (15-2)
(15-2)
В процессе полного горения с теоретически необходимым количеством воздуха образуются газообразные продукты, которые состоят из CO 2 , SO 2 , N 2 и H 2 O - оксиды углерода и серы являются сухими трехатомными газами. Их принято объединять и обозначать через RO 2 = CO 2 + SO 2 .
При горении твердых и жидких топлив теоретические объемы продуктов сгорания, м 3 /кг, вычисляют по уравнениям (15-1) с учетом содержания соответствующих компонентов в топливе и воздухе.
Объем трехатомных газов в соответствии с уравнениями (15-1, а и б)
Теоретический объем азота равен объему азота, поступившему с воздухом 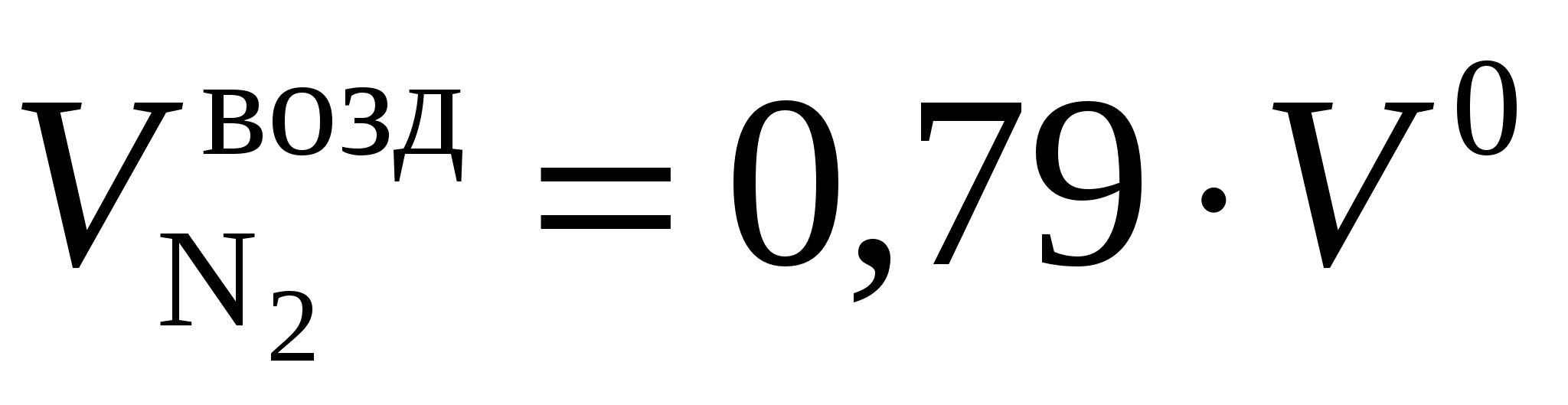 , и объему азота, выделяемого из топлива
, и объему азота, выделяемого из топлива 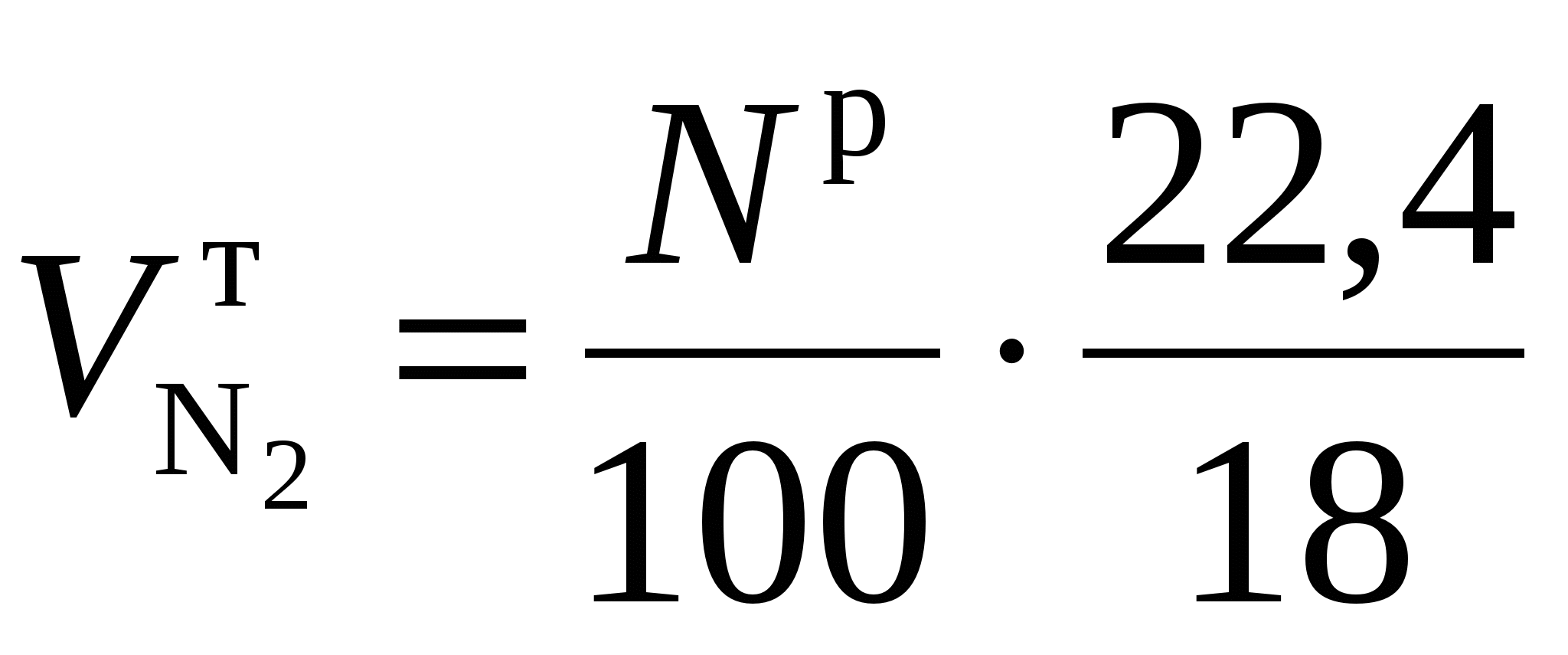 , т. е.
, т. е.
Теоретический объем водяного пара 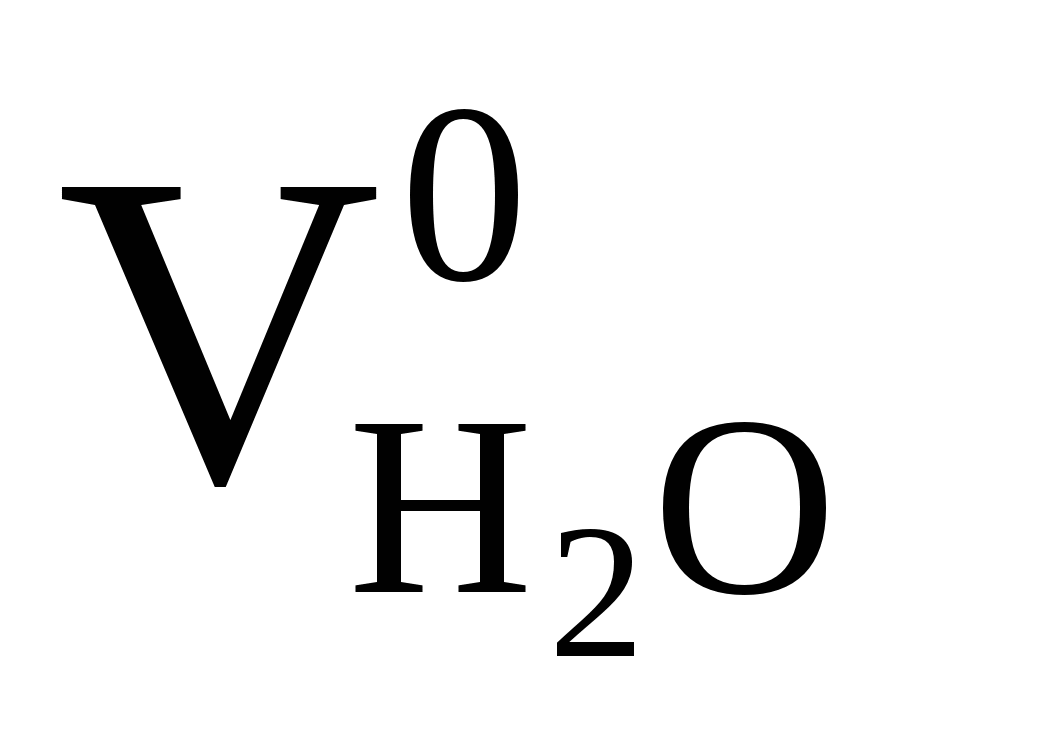 ,
м 3 /кг, складывается из объема, полученного при горении водорода, равного (22,4/2,02)(H р /100), объема, полученного при испарении влаги топлива, равного
,
м 3 /кг, складывается из объема, полученного при горении водорода, равного (22,4/2,02)(H р /100), объема, полученного при испарении влаги топлива, равного 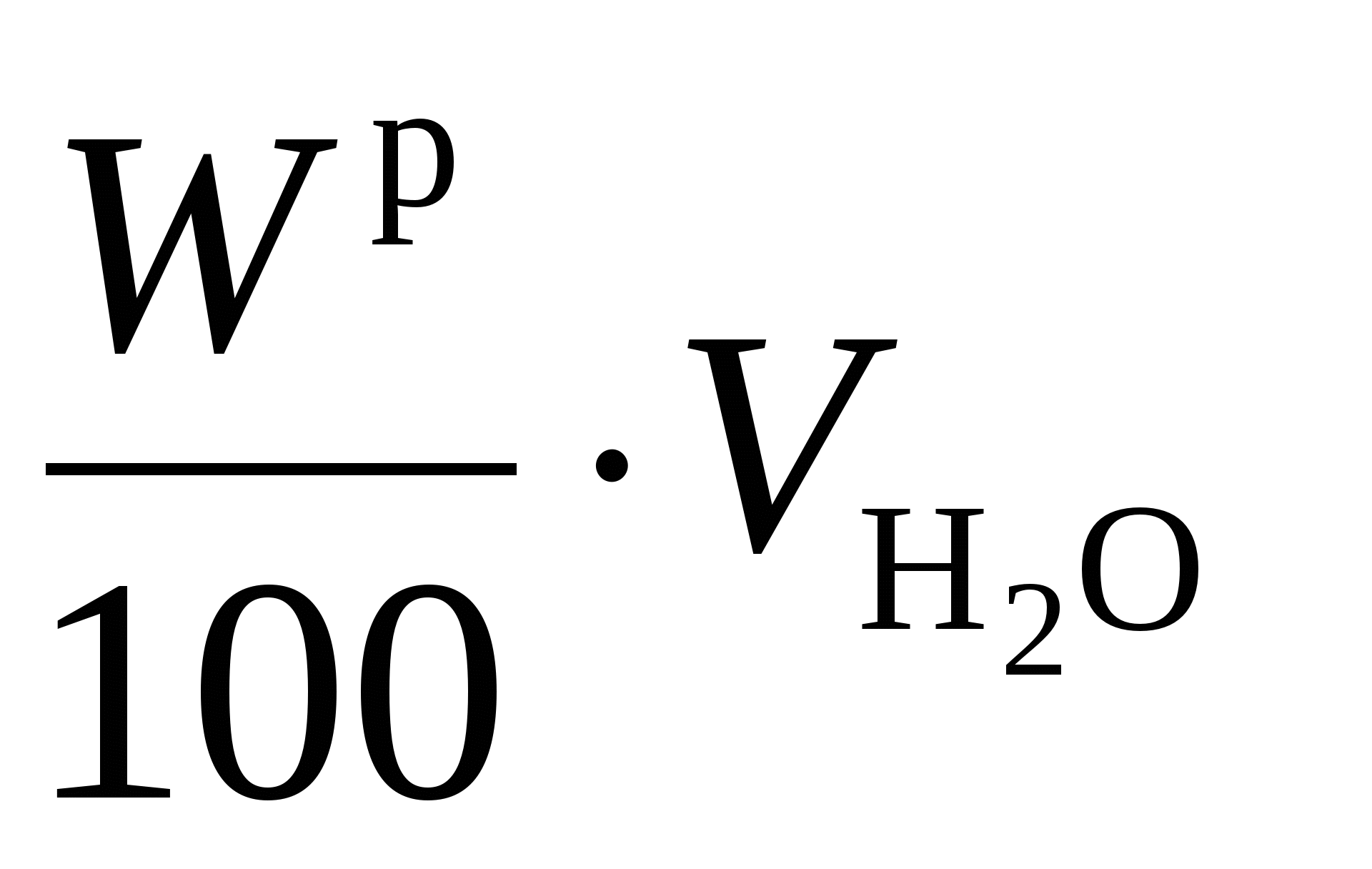 , и объема, вносимого с воздухом:
, и объема, вносимого с воздухом: 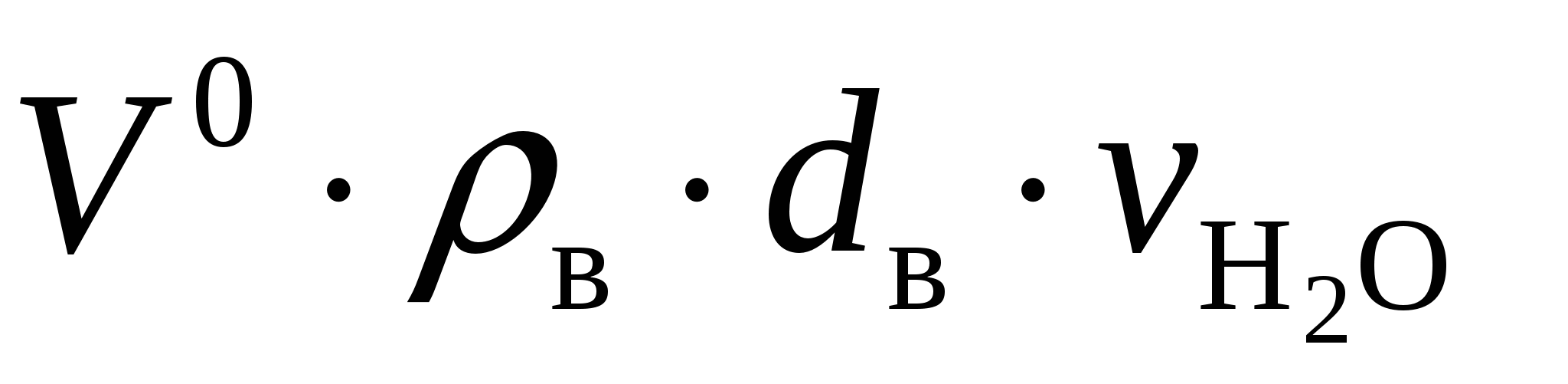 ,
, 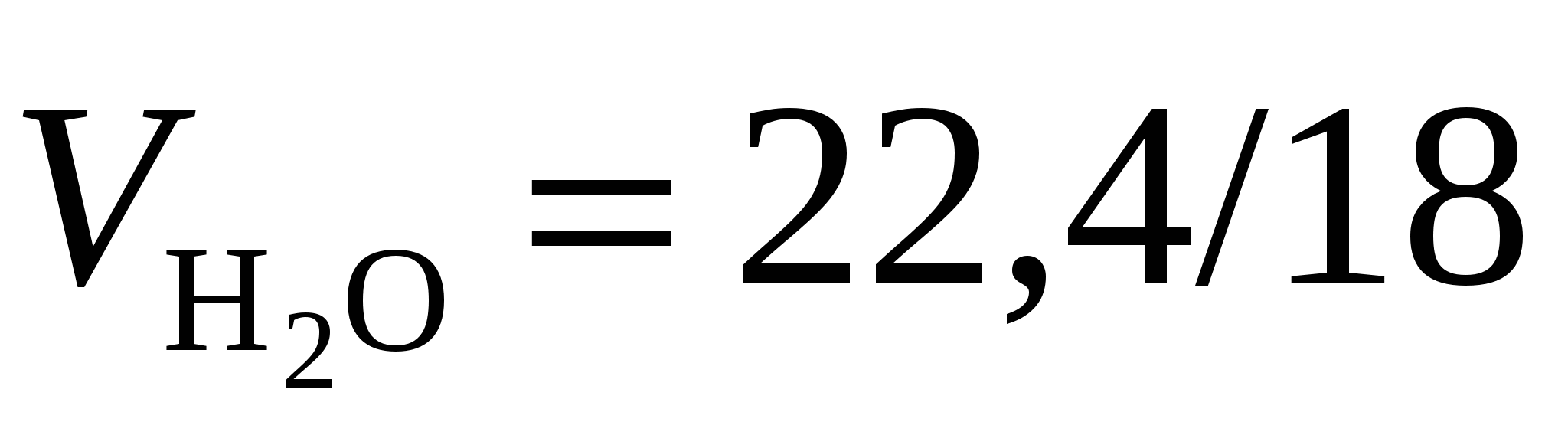
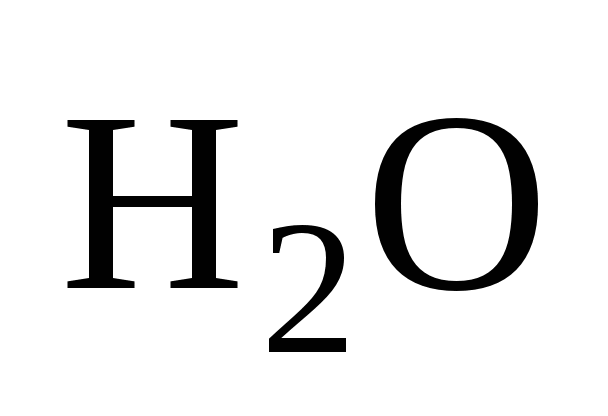
- удельный объем водяного пара, m
3
/
k
г;
в = 1,293 кг/м 3 - плотность воздуха, d
в = 0,01 - содержание влаги в воздухе кг/кг. После преобразований получим:
При паровом распылении мазута теоретический объем водяного пара увеличивают на объем водяного пара, подаваемого в форсунку: 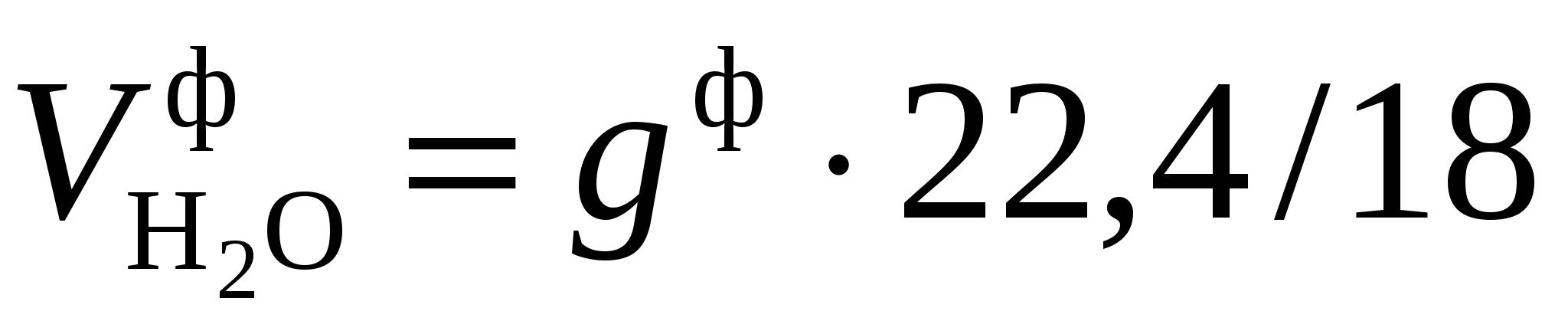 , где
, где 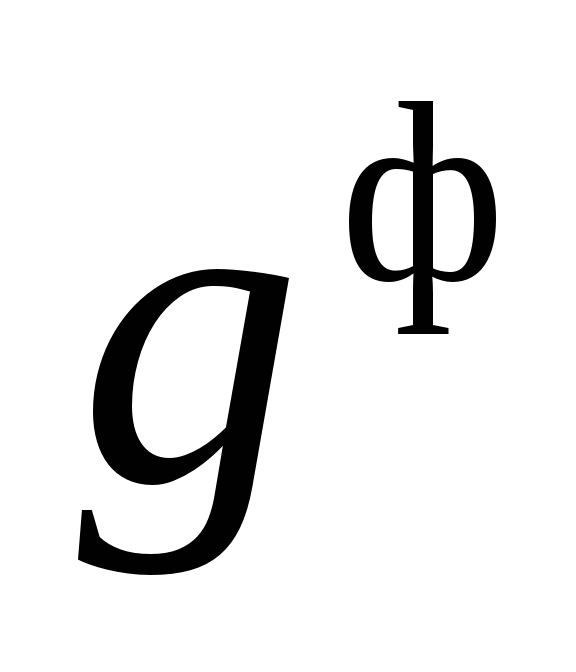 - удельный расход пара на распыление мазута, кг/кг.
- удельный расход пара на распыление мазута, кг/кг.
Суммарный теоретический объем продуктов сгорания, м 3 /кг:
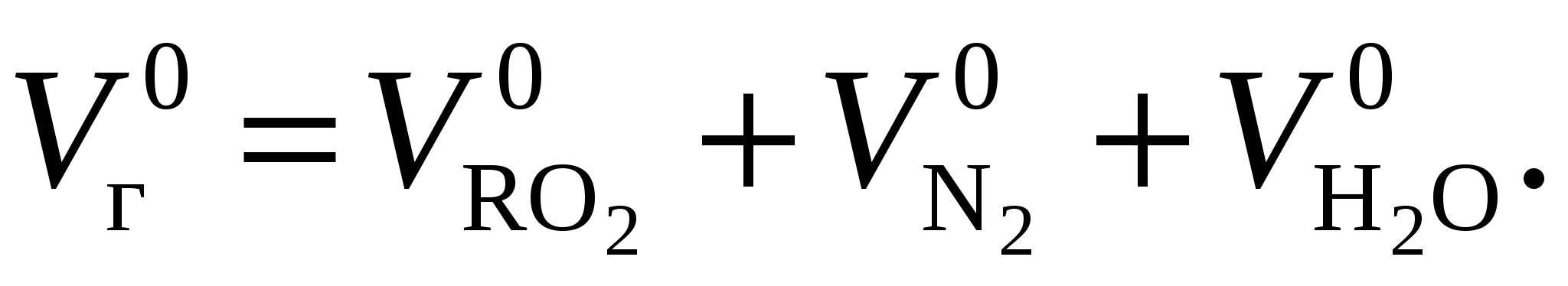 (15-6)
(15-6)
Действительный объем воздуха V может быть больше или меньше теоретически необходимого, подсчитанного по уравнениям горения. Отношение действительного объема воздуха V к теоретически необходимому V 0 называется коэффициентом расхода воздуха = V/V 0 . При > 1 коэффициент расхода воздуха обычно называется коэффициентом избытка воздуха.
Для каждого вида топлива оптимальное значение коэффициента избытка воздуха в топке зависит от технических его характеристик, способа сжигания, конструкции топки, способа образования горючей смеси и др.
Действительный объем продуктов сгорания будет больше теоретического за счет азота, кислорода и водяного пара, который содержится в избыточном воздухе. Так как воздух не содержит трехатомных газов, то их объем не зависит от коэффициента избытка воздуха и остается постоянным, равным теоретическому, т. е. 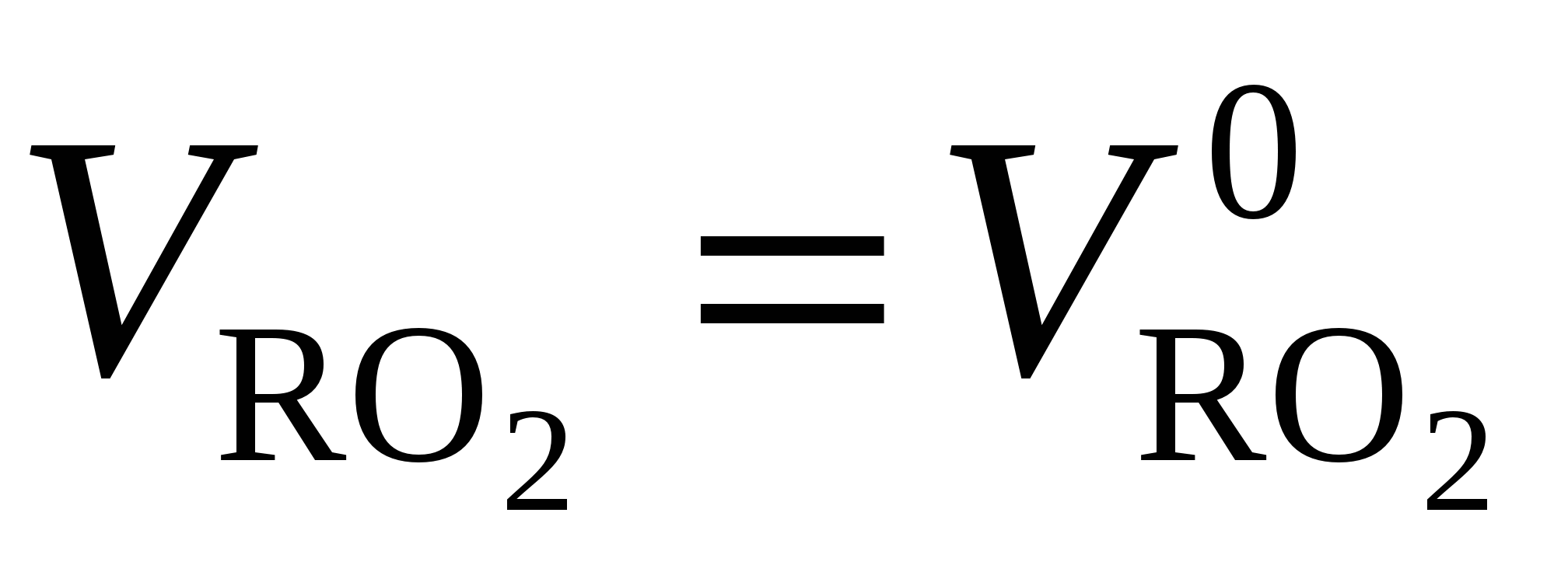 .
.
Объем двухатомных газов и водяного пара (м 3 /кг или м 3 /м 3), определяют по формулам:
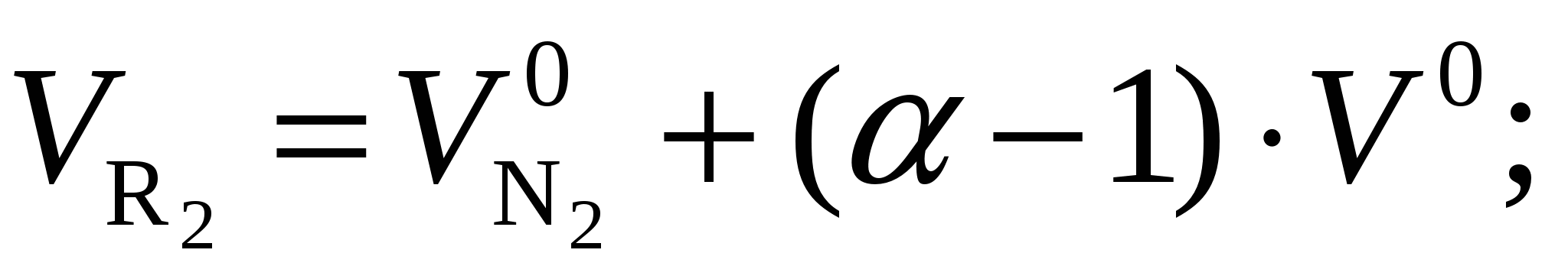 (15-7)
(15-7)
Суммарный объем продуктов сгорания при > 1 (m 3 / k г или м 3 /м 3) будет:
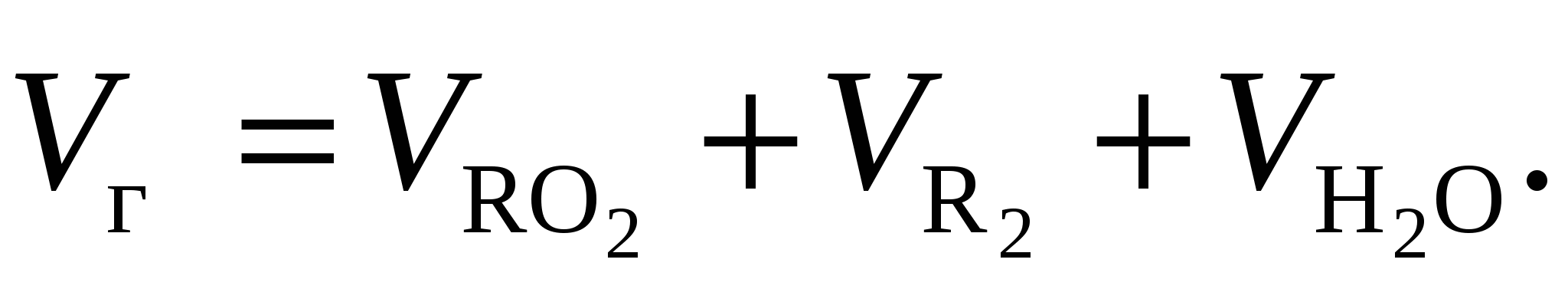 (15-9)
(15-9)
При сжигании твердых топлив концентрация золы в дымовых газах (г/м 3) определяется по формуле
 (15-10)
(15-10)
где  - доля золы топлива, уносимая газами (ее значение зависит от вида твердого топлива и способа его сжигания и принимается из технических характеристик топок).
- доля золы топлива, уносимая газами (ее значение зависит от вида твердого топлива и способа его сжигания и принимается из технических характеристик топок).
Объемные доли сухих трёхатомных газов и водяного пара, равные их парциальным давлениям при общем давлении 0,1 МПа, подсчитывают по формулам
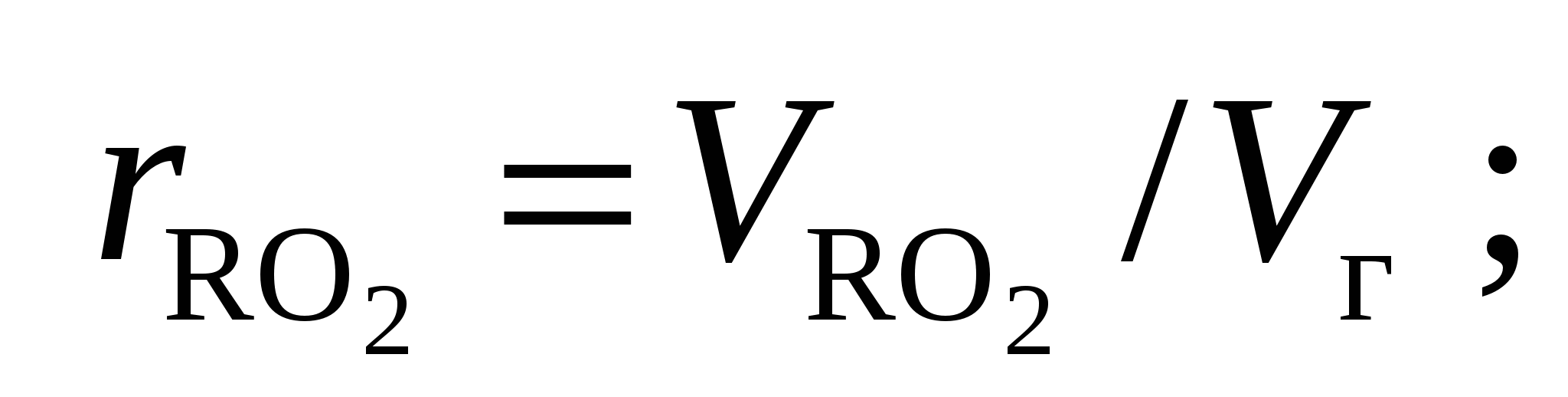
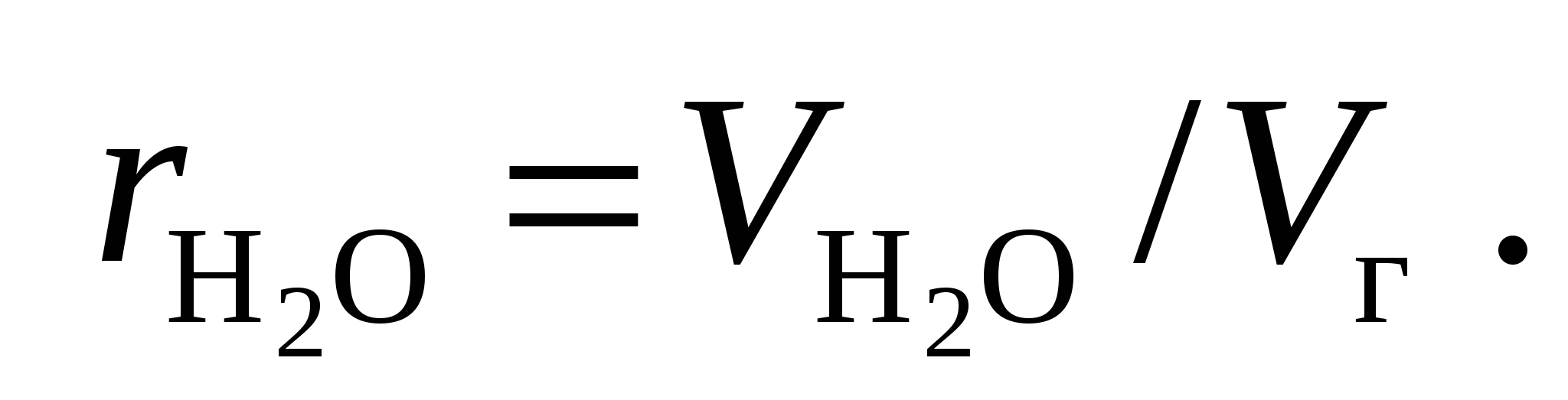
Все формулы для подсчета объемов применимы тогда, когда происходит полное сгорание топлива. Эти же формулы с достаточной для расчета точностью применимы и для неполного сгорания топлива, если не превышаются нормативные значения, приведенные в технических характеристиках топок.
15.2. Три стадии горения твердого топлива
Горение твердого топлива имеет ряд стадий: подогрев, подсушка топлива, возгонка летучих и образование кокса, горение летучих и кокса. Из всех этих стадий определяющей является стадия горения коксового остатка, т. е. стадия горения углерода, интенсивность которой и определяет интенсивность топливосжигания и газификации в целом. Определяющая роль горения углерода объясняется следующим.
Во-первых, твердый углерод, содержащийся в топливе, является главной горючей составляющей почти всех натуральных твердых топлив. Так, например, теплота сгорания коксового остатка антрацита составляет 95% теплоты сгорания горючей массы. С увеличением выхода летучих доля теплоты сгорания коксового остатка падает и в случае торфа составляет 40,5% теплоты сгорания горючей массы.
Во-вторых, стадия горения коксового остатка оказывается наиболее длительной из всех стадий и может занимать до 90% всего времени, необходимого для горения.
И, в третьих, процесс горения кокса имеет решающее значение в создании тепловых условий протекания других стадий. Следовательно, основой правильного построения технологического метода сжигания твердых топлив является создание оптимальных условий для процесса горения углерода.
В некоторых случаях определяющими процесс горения могут оказаться второстепенные подготовительные стадии. Так, например, при сжигании высоко влажного топлива определяющей может быть стадия подсушки. В этом случае рациональным является усиление предварительной подготовки топлива к сжиганию, например, использованием технологического способа сжигания с подсушкой топлива газами, отбираемыми из топки.
В мощных парогенераторах расходуются большие количества топлива и воздуха. Например, для парогенератора 300 МВт расход топлива - антрацитового штыба составляет 32 кг/с, а воздуха 246 м 3 /с а в парогенераторе блока 800 МВт ежесекундно расходуется 128 кг березовского угля и 555 м 3 воздуха. В ряде случаев в пылеугольных парогенераторах как резервное используется жидкое или газовое топливо.
Процесс горения пылевидных топлив совершается в объеме топочной камеры в потоках больших масс топлива и воздуха, к которым подмешиваются продукты сгорания.
Основой горения пылевидных топлив является химическое реагирование горючих составляющих топлива с кислородом воздуха. Однако химические реакции горения в топочной камере протекают в мощных пылегазовоздушных потоках за чрезвычайно короткое время (1-2 с) пребывания топлива и окислителя в топочной камере. Эти реакции совершаются в условиях сильного взаимного влияния с одновременно протекающими физическими процессами. Такими процессами являются:
Процесс движения подаваемых в топочную камеру составляющих горючую смесь газовых и твердых диспергированных веществ в системе струй, переходящих в поток и распространяющихся в ограниченном пространстве топочной камеры с развитием вихревых течений, в совокупности составляющих сложную структуру аэродинамики топки;
Турбулентная и молекулярная диффузия и конвективный перенос исходных веществ и продуктов реакции в газовом потоке, а также перенос газовых реагентов к диспергированным частицам;
Теплообмен в газовых потоках продуктов сгорания и исходной смеси и между газовыми потоками и содержащимися в них частицами топлива, а также передача тепла, выделяющегося при химическом превращении в реагирующей среде;
Радиационный теплообмен частиц с газовой средой и пылегазовоздушной смеси с экранными поверхностями в топочной камере;
Нагрев частиц, возгонка летучих, перенос и горение их в газовом объеме и др.
Таким образом, горение угольной пыли является сложным физико-химическим процессом, состоящим из химических реакций и физических процессов, протекающих в условиях взаимной связи и взаимного влияния.
15.3. Слоевой, факельный и
циклонный способы сжигания твердого
топлива
Топочные устройства котлов могут быть слоевые - для сжигания крупнокускового топлива и камерные - для сжигания газообразного, жидкого и твёрдого пылевидного топлива.
Некоторые из вариантов организации топочных процессов представлены на рис.15.1.
Слоевые топки бывают с плотным и кипящим слоем, камерные подразделяются на факельные и циклонные.
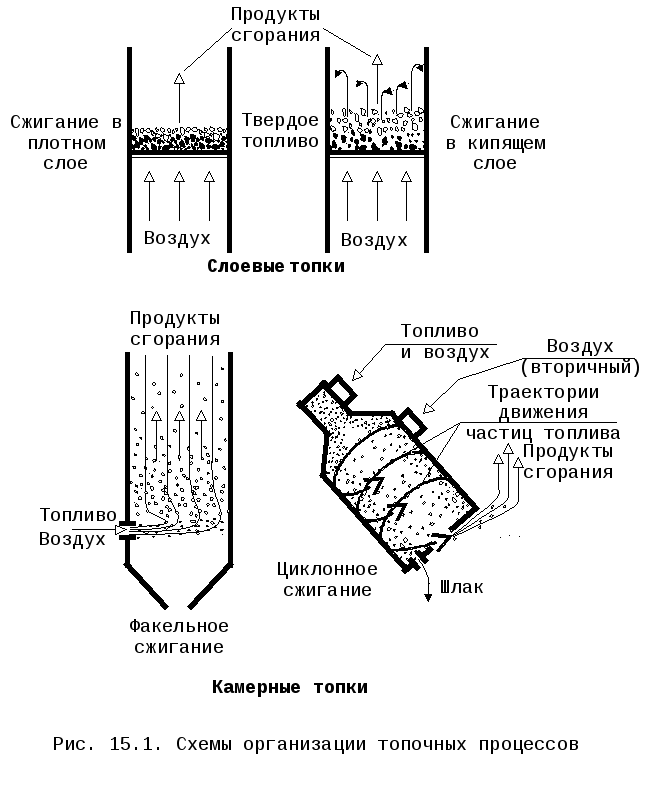
При сжигании в плотном слое воздух для горения проходит через слой, не нарушая его устойчивости, т.е. сила тяжести частиц топлива больше динамического напора воздуха.
При сжигании в кипящем слое из-за повышенной скорости воздуха нарушается устойчивость частиц в слое, они переходят в состояние «кипения», т.е. переходят во взвешенное состояние. При этом происходит интенсивное перемешивание топлива и окислителя, что способствует интенсификации процесса горения.
При факельном сжигании топливо сгорает в объёме топочной камеры, для чего частицы твердого топлива должны иметь размер до 100 мкм.
При циклонном сжигании частицы топлива под влиянием центробежных сил отбрасываются на стенки топочной камеры и, находясь в закрученном потоке в зоне высоких температур, полностью выгорают. Допускается размер частиц больший, чем при факельном сжигании. Минеральная составляющая топлива в виде жидкого шлака удаляется из циклонной топки непрерывно.
15.4. Особенности сжигания жидкого
топлива
Каждое жидкое горючее, так же как любое жидкое вещество, при данной температуре обладает определенной упругостью пара над своей поверхностью, которая увеличивается с ростом температуры.
При зажигании жидкого горючего, имеющего свободную поверхность, загорается его пар, содержащийся в пространстве над поверхностью, образуя горящий факел. За счет тепла, излучаемого факелом, испарение резко увеличивается. При установившемся режиме теплообмена между факелом и зеркалом жидкости количество испаряющегося, а следовательно, и сгорающего горючего достигает максимального значения и далее остается постоянным во времени.
Опыты показывают, что при сжигании жидких топлив со свободной поверхностью горение протекает в паровой фазе; факел устанавливается на некотором удалении от поверхности жидкости и ясно видна темная полоска, отделяющая факел от обреза тигля с жидким горючим. Интенсивность излучения зоны горения на зеркало испарения не зависит от его формы и величины, а зависит только от физико-химических свойств горючего и является характерной константой для каждого жидкого горючего.
Температура жидкого горючего, при которой пары над его поверхностью образуют с воздухом смесь, способную воспламениться при поднесении источника зажигания, называется температурой вспышки.
Поскольку жидкие горючие сгорают в паровой фазе, то при установившемся режиме скорость горения определяется скоростью испарения жидкости с ее зеркала.
Процесс горения жидких горючих со свободной поверхностью происходит следующим образом. При установившемся режиме горения за счет тепла, излучаемого факелом, жидкое горючее испаряется. В восходящий поток горючего, находящегося в паровой фазе, посредством диффузии проникает воздух из окружающего пространства. Полученная таким образом смесь образует горящий факел в виде конуса, отстоящего от зеркала испарения на 0,5-1 мм. Устойчивое горение протекает на поверхности, где смесь достигает пропорции, соответствующей стехиометрическому соотношению горючего и воздуха. Это предположение следует из тех же соображений, что и в случае диффузионного горения газа. Химическая реакция протекает в очень тонком слое фронта факела, толщина которого не превышает нескольких долей миллиметра. Объем, занимаемый факелом, зоной горения делится на две части: внутри факела находятся пары горючей жидкости и продукты сгорания, а вне зоны горения -смесь продуктов горения с воздухом.
Горение восходящих внутри факела паров жидких топлив можно представить состоящим из двух стадий: диффузионного подвода кислорода к зоне горения и самой химической реакции, протекающей во фронте пламени. Скорости этих двух стадий не одинаковы; химическая реакция при имеющих место высоких температурах протекает очень быстро, тогда как диффузионный подвод кислорода является медленным процессом, ограничивающим общую скорость горения. Следовательно, в данном случае горение протекает в диффузионной области, а скорость горения определяется скоростью диффузии кислорода в зону горения.
Так как условия подвода кислорода к зоне горения при сжигании различных жидких горючих со свободной поверхности примерно одинаковы, следует ожидать, что скорость их горения, отнесенная к фронту пламени, т. е. к боковой поверхности факела, также должна быть одинаковой. Длина факела будет тем больше, чем больше скорость испарения.
Специфической особенностью горения жидких горючих со свободной поверхности является большой химический недожог. Каждое горючее, представляющее собой углеродистое соединение при сжигании со свободной поверхности, имеет свойственную ему величину химического недожота, которая составляет, %:
Для спирта......... 5,3
Для керосина........ 17,7
Для бензина........ 12,7
Для бензола......... 18,5.
Картину возникновения химического недожога можно представить следующим образом.
Парообразные углеводороды при движении внутри конусообразного факела до фронта пламени при нахождении в области высоких температур при отсутствии кислорода, подвергаются термическому разложению вплоть до образования свободного углерода и водорода.
Свечение пламени обусловливается нахождением в нем частиц свободного углерода. Последние, раскалившись за счет выделяемого при горении тепла, излучают более или менее яркий свет.
Часть свободного углерода не успевает сгорать и в виде сажи уносится продуктами сгорания, образуя коптящий факел.
Кроме того, наличие углерода вызывает образование СО.
Высокая температура и пониженное парциальное давление СО и СО 2 в продуктах сгорания благоприятствуют образованию СО.
Присутствующие в продуктах сгорания количества углерода и СО обусловливают величину химического недожога. Чем больше содержание углерода в жидком топливе и чем меньше он насыщен водородом, тем больше образование чистого углерода, ярче факел, больше химический недожог.
Таким образом, исследования горения жидких горючих со свободной поверхности показали, что:
1) горение жидких топлив происходит после их испарения в паровой фазе. Скорость горения жидких топлив со свободной поверхности определяется скоростью их испарения за счет тепла, излучаемого зоной горения, при установившемся режиме теплообмена между факелом и зеркалом испарения;
2) скорость горения жидких горючих со свободной поверхности растет с увеличением температуры их подогрева, с переходом к горючим с большей интенсивностью излучения зоны горения, меньшей теплотой парообразования и теплоемкостью и не зависит от величины и формы зеркала испарения;
3) интенсивность излучения зоны горения на зеркало испарения, горящего со свободной поверхности жидкого горючего, зависит только от его физико-химических свойств и является характерной константой для каждого жидкого горючего;
4) теплонапряжение фронта диффузионного факела над поверхностью испарения жидкого горючего практически не зависит от диаметра тигля и рода топлива;
5) горению жидких горючих со свободной поверхности присущ повышенный химический недожог, величина которого характерна для каждого горючего.
Имея в виду, что горение жидких топлив происходит в паровой фазе процесс горения капли жидкого горючего можно представить следующим образом.
Капля жидкого топлива окружена атмосферой, насыщенной парами этого горючего. Вблизи от капли по сферической поверхности устанавливается зона горения. Химическое реагирование смеси паров жидкого топлива с окислителем происходит весьма быстро, поэтому зона горения весьма тонка. Скорость горения определяется наиболее медленной стадией - скоростью испарения горючего.
В пространстве между каплей и зоной горения находятся пары жидкого топлива и продукты горения. В пространстве вне зоны горения - воздух и продукты сгорания.
В зону горения изнутри диффундируют пары топлива, а снаружи - кислород. Здесь эти компоненты смеси вступают в химическую реакцию, которая сопровождается выделением тепла. Из зоны горения тепло переносится наружу и к капле, а продукты сгорания диффундируют в окружающее пространство и в пространство между зоной горения и каплей. Однако механизм передачи тепла еще не представляется ясным.
Ряд исследователей считает, что испарение горящей капли происходит за счет молекулярного переноса тепла через застойную пограничную пленку у поверхности капли.
По мере выгорания капли из-за уменьшения поверхности общее испарение уменьшается, зона горения суживается и исчезает при полном выгорании капли.
Так протекает процесс горения капли полностью испаряющихся жидких топлив, находящейся в покое в окружающей среде или движущейся вместе с ней с одинаковой скоростью.
Количество кислорода, диффундирующее к шаровой поверхности при прочих равных условиях, пропорционально квадрату ее диаметра, поэтому установление зоны горения на некотором удалении от капли обусловливает большую скорость ее горения по сравнению с такой же частицей твердого топлива, при горении которой химическая реакция практически протекает на самой поверхности.
Так как скорость горения капли жидкого топлива определяется скоростью испарения, то время ее выгорания можно рассчитать на основе уравнения теплового баланса ее испарения за счет тепла, получаемого из зоны горения.
Так как горение жидких топлив происходит после их испарения в паровой фазе, то его интенсификация связана с интенсификацией испарения и смесеобразования. Это достигается за счет увеличения поверхности испарения путем распыления жидкого топлива на мельчайшие капельки и хорошего смешения образовавшихся паров с воздухом при равномерном распределении мелкодисперсного топлива в нем. Эти две задачи выполняют, применяя горелки с форсунками, которыми распыляют жидкое топливо в потоках воздуха, подаваемых в камерную топку через воздухонаправляющие аппараты горелок.
Воздух, необходимый для горения, подается в устье форсунки, захватывает тонко распыленное жидкое топливо и образует в топочной камере неизотермическую затопленную струю. Струя, распространяясь, нагревается за счет увлечения продуктов сгорания высокой температуры. Мельчайшие капельки жидкого топлива, нагреваясь благодаря конвективному теплообмену в струе, испаряются. Нагрев распыленного топлива происходит также за счет поглощения ими тепла, излучаемого топочными газами и раскаленной обмуровкой.
На начальном участке и в особенности в пограничном слое струи интенсивный нагрев факела вызывает быстрое испарение капель. Пары горючего, смешиваясь с воздухом, создают газовоздушную горючую смесь, которая, воспламеняясь, образует факел.
Таким образом, процесс горения жидкого топлива можно разбить на следующие фазы: распыление жидкого топлива, испарение и образование газовоздушной смеси, воспламенение горючей смеси и горение последней.
Температура и концентрация газовоздушной смеси изменяются по сечению струи. По мере приближения к внешней границе струи температура повышается, а концентрация компонентов горючей смеси падает. Скорость распространения пламени в паровоздушной смеси зависит от состава, концентрации и температуры и достигает максимальной величины в наружных слоях струи, где температура близка к температуре окружающих топочных газов несмотря на то, что здесь горючая смесь сильно разбавлена продуктами сгорания. Поэтому воспламенение в мазутном факеле начинается у корня с периферии и затем распространяется вглубь струи на все сечение, достигая ее оси на значительном расстоянии от форсунки, равном перемещению центральных струй за время распространения пламени от периферии до оси. Зона воспламенения принимает форму вытянутого конуса, основание которого находится на малом расстоянии от выходного сечения амбразуры горелки.
Положение зоны воспламенения зависит от скорости смеси; зона занимает такое положение, при котором во всех ее точках устанавливается равновесие между скоростью распространения пламени и скоростью движения. Центральные струи, имеющие наибольшую скорость, затухают по мере продвижения в топочном пространстве, определяя длину зоны воспламенения местом, где скорость падает до абсолютной величины скорости распространения пламени.
Горение основной части парообразных углеводородов происходит в зоне воспламенения, занимающей наружный слой факела небольшой толщины. Горение высокомолекулярных углеводородов, сажи, свободного углерода и неиспарившихся капель жидкого топлива продолжается за зоной воспламенения и требует определенного пространства, обусловливая общую длину факела.
Зона воспламенения делит пространство, занимаемое факелом, на две области: внутреннюю и наружную. Во внутренней области протекает процесс испарения и образования горючей смеси.
Во внутренней области парообразные углеводороды подвергаются нагреву, который сопровождается окислением и расщеплением их. Процесс окисления начинается при сравнительно низких температурах- порядка 200-300°С. При температурах 350-400°С и выше наступает процесс термического расщепления.
Процесс окисления углеводородов благоприятствует последующему процессу горения, так как при этом выделяется некоторое количество тепла и повышается температура, а наличие кислорода в составе углеводородов способствует дальнейшему их окислению. Напротив, процесс термического расщепления является нежелательным, так как образующиеся при этом высокомолекулярные углеводороды сгорают трудно.
Из нефтяных топлив в энергетике применяется лишь мазут. Мазут представляет собой остаток от перегонки нефти при температуре порядка 300°С, но ввиду того, что процесс перегонки происходит не полностью, мазут при температурах ниже 300°С еще выделяет некоторое количество паров более легких погонов. Поэтому при входе распыленной струи мазута в топку и постепенном нагревании часть его превращается в пары, а часть еще может находиться в жидком состоянии даже при температуре порядка 400°С.
Поэтому при сжигании мазута необходимо способствовать протеканию окислительных реакций и всемерно препятствовать термическому разложению при высоких температурах. Для этого весь воздух, необходимый для горения, следует подавать в корень факела. В этом случае наличие большого количества кислорода во внутренней области будет, с одной стороны, благоприятствовать окислительным процессам, а с другой - понижать температуру, что обусловит расщепление молекул углеводородов более симметрично без образования значительного количества трудно сжигаемых высокомолекулярных углеводородов.
Смесь, получающаяся при сжигании мазута, содержит паро- и газообразные углеводороды, жидкие более тяжелые погоны, а также твердые соединения, образующиеся в результате расщепления углеводородов (т. е. все три фазы-газообразную, жидкую и твердую). Паро- и газообразные углеводороды, смешиваясь с воздухом, образуют горючую смесь, горение которой может протекать по всем возможным способам горения газов. Аналогично сгорает и СО, образовавшийся при горении жидких капель и кокса.
В факеле зажигание капель осуществляется за счет конвективного нагрева; вокруг каждой капли устанавливается зона горения. Горение капли сопровождается химическим недожогом в виде сажи и СО. Капли высокомолекулярных углеводородов при горении дают твердый остаток - кокс.
Образующиеся в факеле твердые соединения - сажа и кокс сгорают так же, как происходит гетерогенное горение частиц твердого топлива. Наличие накаленных частиц сажи обусловливает свечение факела.
Свободный углеводород и сажа в среде с высокой температурой при наличии достаточного количества воздуха могут сгореть. В случае же местного недостатка воздуха или недостаточно высокой температуры они сгорают не полностью с определенной химической неполнотой горения, окрашивая продукты сгорания в черный цвет - коптящий факел.
Зона догорания газообразных продуктов неполного сгорания и твердых частиц, следующая за зоной горения, увеличивает общую длину факела.
Химический недожог, характерный для горения жидких топлив со - свободной поверхности при сжигании их в факеле, соответствующими режимными мероприятиями может и должен быть сведен практически к нулю.
Таким образом, для интенсификации сжигания мазута необходимо хорошее распыление. Предварительный подогрев воздуха и мазута способствует газификации мазута, поэтому будет благоприятствовать зажиганию и горению. Весь воздух, необходимый для горения, следует подавать в корень факела. При этом рациональной конструкцией воз-духонаправляющего устройства горелки, правильной установкой форсунки и соответствующей конфигурацией амбразуры горелки необходимо обеспечить хорошее перемешивание распыленного топлива с воздухом, а также перемешивание в горящем факеле и в особенности в конечной его части. Температура в факеле должна поддерживаться на достаточно высоком уровне и для обеспечения интенсивного завершения процесса горения в конце факела должна быть не ниже 1000-1050°С.
Факелу должно быть обеспечено достаточное пространство для развития процесса горения, так как в случае соприкосновения продуктов сгорания (до завершения процесса горения) с холодными поверхностями нагрева парогенератора температура может настолько понизиться, что содержащиеся в газах не догоревшие частицы сажи и свободного углерода, а также высокомолекулярные углеводороды не смогут гореть.
Процесс горения нефтяного факела в закрученной струе протекает аналогично рассмотренному случаю при прямоточной струе. При закрученном движении на оси струи создается зона разрежения, вызывающая приток горячих продуктов сгорания к корню факела. Это обеспечивает устойчивое зажигание.
Использование центробежного эффекта в механических и вращающихся форсунках приводит к разрыву сплошного потока. Жидкость внутри выходного канала форсунки принимает форму полого цилиндра, заполненного парами и газами. Из сопла вытекает эмульсия, образуя жидкую пленку в виде раскрывающегося гиперболоида. В направлении движения сечение гиперболоида увеличивается, а пленка жидкости утоньшается, начинает пульсировать и, наконец, распадается на быстродвижущиеся капельки, которые в потоке подвергаются дальнейшему измельчению.
В паровых форсунках первичное дробление производится за счет кинетической энергии пара, истекающего из сопла форсунки. Капли первичного дробления приобретают скорость паровой струи, обычно соответствующую критической скорости.
15.5. Сжигание топлива и защита
окружающей среды
15.5.1. Черная металлургия как источник загрязнения окружающей среды
Металлургический завод, производящий 1 млн. т. стали в год, за сутки выбрасывает в атмосферу 350 т. пыли, 400 т. окиси углерода и 200 т. двуокиси серы. От общего количества выбросов на долю металлургических заводов приходится 20% выбросов пыли, 43% окиси углерода, 16% сернистого ангидрида и 23% окислов азота. Больше всего выбросов у аглофабрики и ТЭЦ. От общего количества выбросов металлургического завода аглофабрика даёт 34% пыли, 82% сернистого ангидрида, 23% окислов азота. ТЭЦ выбрасывает 36% пыли. Таким образом, аглофабрика и ТЭЦ вместе выбрасывают в атмосферу около 70% общезаводских выбросов пыли.
Различают очистку газов от взвешенных твёрдых частиц (пыли) и улавливание вредных газообразных веществ химическими методами газоочистки. В настоящее время очистка выбрасываемых в атмосферу газов от вредных газообразных веществ почти не применяется (и не только у нас) за исключением коксохимического производства, где такая очистка широко распространена в связи необходимостью улавливания ряда ценных веществ.
На заводах чёрной металлургии, главным образом, осуществляют механическую очистку газов от пыли. По принципу действия применяемые методы очистки делят на сухие и мокрые. Мокрые пылеуловители позволяют одновременно с улавливанием пыли частично очищать газы от диоксида серы (SO 3). Однако эти пылеуловители повышают расход воды и требуют применения устройств для её очистки.
15.5.2. Аппараты для сухой механической очистки газов
Делятся на пылеуловители и фильтры. В свою очередь пылеуловители подразделяются на гравитационные и инерционные. Гравитационные пылеуловители имеют пылевые камеры различной конструкции. В этих пылеуловителях осаждение пыли происходит, в основном, под действием сил тяжести. Силы инерции здесь оказывают незначительное влияние на процесс извлечения пыли из потока газа.
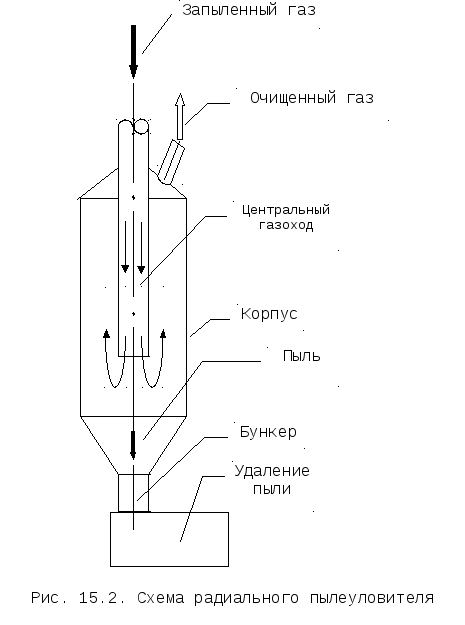 На рисунке 15.2 приведена схема радиального пылеуловителя. В него через центральный газоход поступает запыленный
На рисунке 15.2 приведена схема радиального пылеуловителя. В него через центральный газоход поступает запыленный
газ, который в бункере снижает скорость своего движения и меняет направление движения на 180 0 . Пыль, содержащаяся в газе, под действием сил тяжести и по инерции, оседает в бункере, а газ удаляется в очищенном виде.
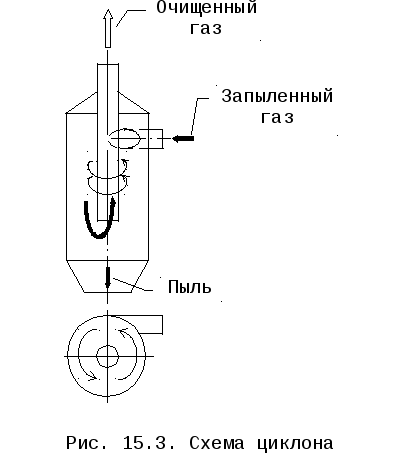
Гравитационные пылеуловители эффективны при удалении частиц пыли с размерами большими 100 мкм, т.е. достаточно крупных частиц.
В инерционных (центробежных) пылеуловителях на частицы пыли действует сила инерции, возникающая при повороте или вращении газового потока. Так как эта сила значительно превосходит гравитационную, то и удаляются из газового потока частицы более мелкие, чем при гравитационной очистке.
Пример такого пылеуловителя - циклон, удаляющий из газового потока частицы пыли с размерами большими 20 мкм. Запыленный газовый поток вводится в верхнюю часть корпуса циклона через патрубок, расположенный тангенциально относительно корпуса. Поток приобретает вращательное движение, тяжелые частицы пыли силами инерции отбрасываются к стенкам циклона и под действием сил тяжести опускаются в бункер, а очищенный газ удаляется из циклона.
Фильтры - это аппараты, обеспечивающие тонкую очистку газа. По типу фильтрующего элемента подразделяются на фильтры с волокнистым фильтрующим элементом, с тканевым, зернистым, металлокерамическим, керамическим. Типичным примером являются фильтры с тканным фильтрующим элементом: из натуральных и синтетических тканей или металлотканый, выдерживающий температуру до 600 0 С.
Регенерация тканевого фильтра осуществляется обратной продувкой сжатым воздухом.
Запыленный газ проходит через рукавную ткань, оставляя на ней частички пыли, и очищенным удаляется из фильтра. Пыль оседает в бункер по мере её накопления на ткани. Когда сопротивление ткани существенно возрастает, обратной продувкой воздухом тканевый рукав отчищается от пыли.
15.5.3. Электрофильтры
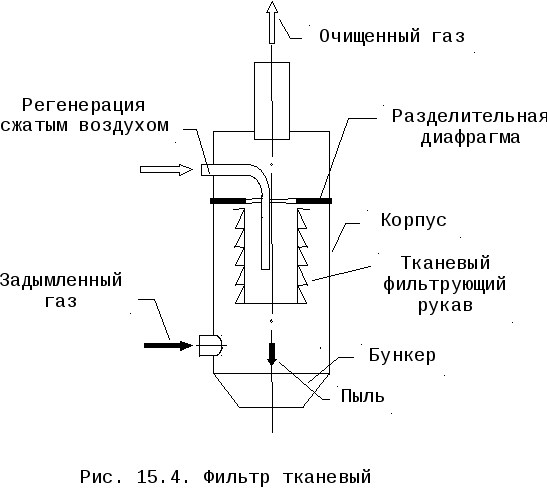
Электрофильтры - аппараты для тонкой очистки газа. Принцип действия этих фильтров основан на силовом взаимодействии заряженных частиц между собой и с металлическими электродами. Вы знаете, что одноимённо заряженные частицы отталкиваются, а разноименно заряженные - притягиваются. В электрофильтре частицы пыли, попадая в электрическое поле, заряжаются и затем под действием сил взаимодействия с осадительными электродами притягиваются к ним, осаждаются на них и теряют свой заряд. В качестве примера рассмотрим работу трубчатого электрофильтра. Фильтр состоит из корпуса и центрального электрода, конструкция которого на схеме не раскрыта. Корпус фильтра заземляется. Центральный электрод состоит из пластин, часть из которых подсоединена к корпусу, а другая часть - изолирована от него.
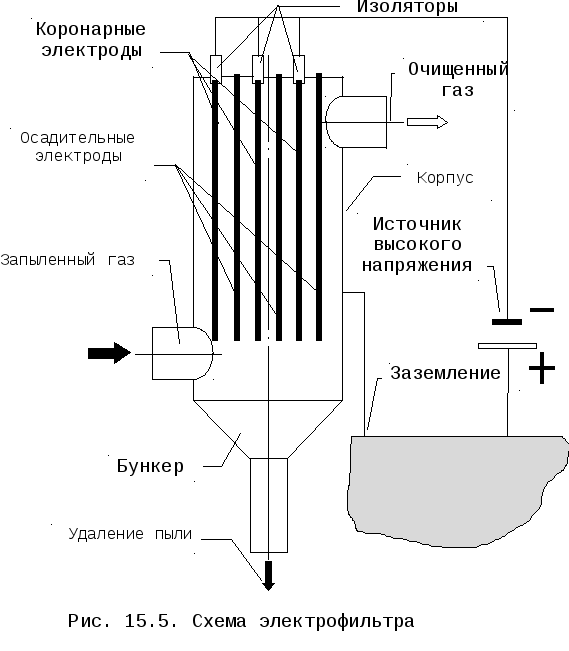
Изолированные и подсоединённые к корпусу электроды чередуются. Между ними создаётся разность потенциалов порядка 25-100 кВ. Величина разности потенциалов определяется геометрией электродов и тем больше, чем больше расстояние между ними. Это связано с тем, что электрофильтр работает, если между электродами существует коронный разряд.
Газ, проходя между электродами, ионизируется. Частицы пыли взаимодействуют с йонами, приобретают отрицательный заряд и притягиваются к осадительным электродам. Осаждаясь на электродах частицы пыли теряют свой заряд и частично осыпаются в бункер.
Производится периодическая очистка фильтра встряхиванием или промывкой. На время очистки фильтр отключается.
При работе на доменном газе фильтр промывают через каждые 8 часов в течение 15 минут. Максимальная температура очищаемого газа не должна превышать 300 0 С. Рабочая температура очищаемого газа 250 0 С. Высота электродов до 12 м.
Электрофильтр очищает газ от частиц пыли с размерами меньшими 1 мкм.
15.5 .4. Мокрая очистка газов
В аппаратах мокрой очистки запыленный газ промывается водой, что позволяет отделить значительную часть пыли.
Наибольшее применение в чёрной металлургии нашли скрубберы различной конструкции и турбулентные газопромыатели.
Скрубберы - это агрегаты, в которых запыленный газ поднимается навстречу орошающей воде. С целью защиты от коррозии внутренние поверхности скруббера футеруются керамической плиткой. Максимальная температура газа в скруббере 300 0 С. Размеры скруббера: диаметр - 6-8 м, высота - 20-30 м. Расход воды - 1,5-2 кг/м 3 газа. В скрубберах осуществляется полутонкая очистка от пыли.
Скоростной газопромыватель - эффективный аппарат тонкой очистки, применяемый как самостоятельно, так и для подготовки газа перед электрофильтром. Состоит из трубы-распылителя и циклона каплеуловителя. Улавливает частицы пыли размерами до 0,1 мкм. Производительность по газу 40000 м 3 /ч и более. Удельный расход орошающей воды 0,15-0,5 кг/м 3 . Скорость газа в горловине трубы-распылителя 40-150 м/с.
Принцип действия скоростного газопромывателя основан на улавливании в циклоне мелких частиц пыли утяжелённых смачивающей их водой. Смачивание частиц пыли осуществляется в трубе-распылителе.
В заключение следует отметить, что пыль с частицами крупнее 10-20 мкм хорошо улавливается в большинстве аппаратов газоочистки. Для очистки от пыли с частицами меньшими 1 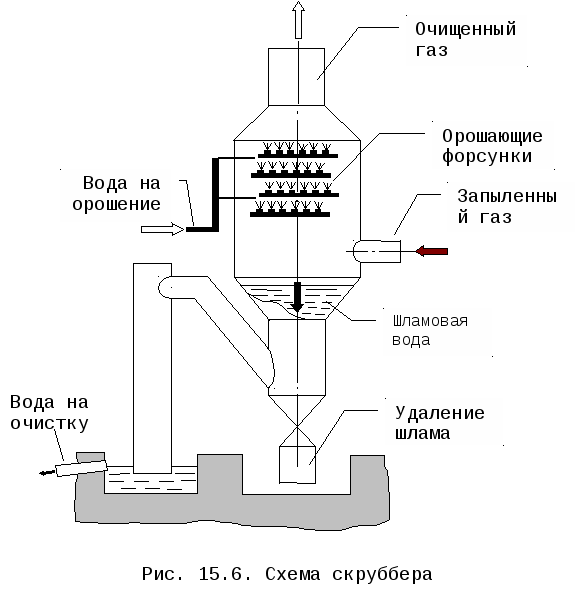
мкм пригодны только аппараты тонкой очистки: пористые фильтры, электрофильтры, скоростные газопромыватели.
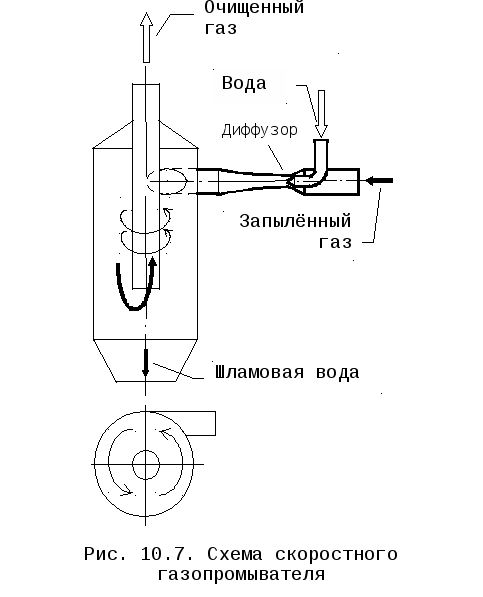
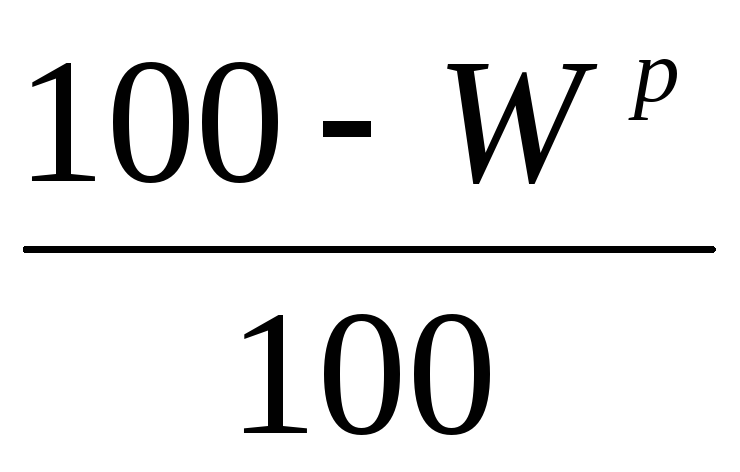 %.
%.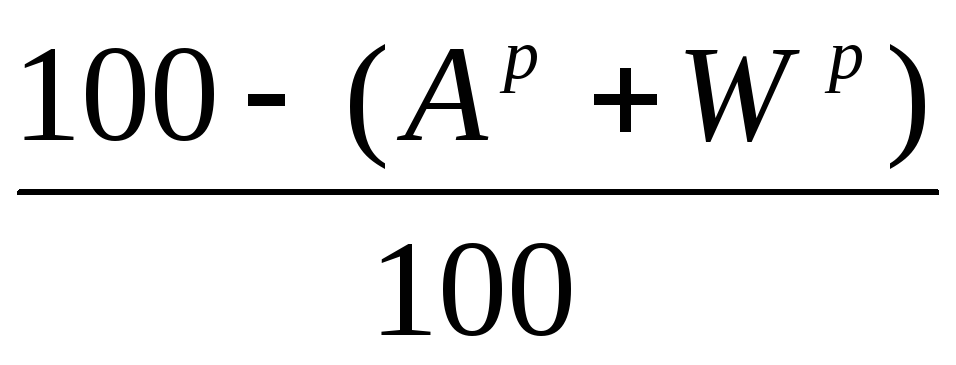 %,
%,